İçindekiler
- “Korozyon“, bir metalin istenmeyen bir şekilde ve kendiliğinden yükseltgenmesidir.
- Korozyon olayına, “metallerin paslanması” da denebilir.
- Yanma tepkimeleri, redoks tepkimeleridir.
- Metallerin paslanması de bir çeşit yanma tepkimesidir. Bu yüzden, metallerin paslanması, bir çeşit redoks tepkimesidir.
- Paslanma esnasında, metaller katyonlara (+ yüklü iyonlara) dönüşür ve oksit bileşikleri oluştururlar.
- Metallerin paslanması, kendiliğinden gerçekleşir. Bu yüzden, paslanma istemli bir redoks tepkimesidir.
- Bazı korozyon olayları şunlardır:
- Demirin paslanması
- Gümüşün kararması
- Bakırın yeşil renge dönüşmesi
Korozyonun Zararları

- Korozyon istenmeyen ve engellenmeye çalışılan bir olaydır.
- Korozyona uğrayan metaller, toz haline dönüşür ve dökülerek suya veya toprağa karışırlar.
- Suya veya toprağa karışan metal paslarını buradan ayırmak çoğu zaman mümkün olmamaktadır.
- Korozyon sebebiyle, dünyada, her yıl tonlarca metal kaybedilmektedir.
- Korozyon sebebiyle, demirden veya diğer metallerden yapılmış araç ve aletler zamanla kullanılamaz hale gelmektedir.
Korozyon Nasıl Gerçekleşir?
- Korozyonun gerçekleşmesine sebep olan başlıca faktör sudur veya nemdir.
- Ancak saf suda korozyon çok yavaş ilerler.
- Hava ile temas eden suda, CO2 gazı çözünür ve su asidik hale geçer.
- Asidik özellik kazanmış suda paslanma daha hızlı gerçekleşir.
Demirin (Fe) Paslanması
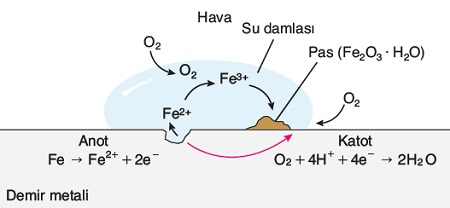
- Demirin paslanması olayında; demir metali, hava ve suyla temas ederek yükseltgenir.
- Paslanma olayında havadaki oksijen gazı indirgenir.
- Yükseltgenme yarı tepkimesinde, Fe metali yükseltgenerek oksit bileşiğine dönüşür.
- Aşağıda, Fe metalinin paslanmasına ait yarı tepkimeler verilmiştir:
- Katot (İYT): O2(g) + 4H+ + 4e– → 2H2O(s)
- Anot (YYT): 2Fe(s) → Fe2+ + 4e–
- Bu tepkimeler ile, yükseltgenen Fe2+ iyonu, havanın oksijeni ile bir daha yükseltgenerek Fe3+ iyonuna dönüşür.
- Fe3+ iyonu ise, oksijen iyonu ile Fe2O3.xH2O
- Demirin pası, Fe2O3.xH2O genel formülü ile gösterilir.
Korozyondan Korunma
- Korozyon, metallerin paslanarak kullanım dışı kalmasına sebep olur.
- Bu yüzden; hem ülke ekonomisine hem de dünyadaki metal kaynaklarına zararı olan bir olaydır.
- Bu yüzden, korozyonun önlenmesi, istenen ve önemli bir olaydır.
Metallerin, korozyona uğramasını engellemenin çeşitli yolları vardır. Bunlar şöyle sıralanabilir:
Metalleri Boyama

- Metallerin boyanması, hem hava ile hem de su ile temasını keseceği için, metallerin paslanmasını önler.
Galvanizleme
- Demir ve çelik malzemelerin üzerine ince bir çinko tabakası kaplama işlemine galvanizleme denir.
- Çinko metali, demir metaline göre daha aktiftir (Daha kolay yükseltgenir.)
- Ancak çinkonun yükseltgenme ürünleri çinkoya sıkıca yapışarak onun daha fazla korozyona uğramasını engeller. Yani demir metalinin hava ve su ile temasını engelleyen koruyucu bir tabaka oluşur.
- Eğer çinko metal tabakası çizilirse ve alttaki demir tabakası açığa çıkarsa bu durumda çinko metali, demir metaline elektron vererek yükseltgenir.
- Böylece demir, çinkonun yükseltgenmesi sayesinde korozyona karşı korunur.
- Bu yönteme galvanize etme denir.
Pasif Metallerle Kaplama
- Bazı metaller, korozyona karşı dayanıklıdır ve paslanmazlar. Bir metalin, korozyona dayanıklı başka bir metal tarafından kaplanması, korozyonu önler.
- Gümüş, altın, bakır, paslanmaz çelik gibi pasif metaller, kaplamacılıkta sık kullanılan metallerdir.

- Yukarıda, bir metal kaşığın gümüş kaplanması için hazırlanmış hücre düzeneği verilmiştir:
- Gümüş metal, hücrenin katotudur
- Metal kaşık hücrenin anotudur.
- Hücrenin elektrolit çözeltisi olarak gümüş tuzu (AgNO3) çözeltisi kullanılmıştır.
- Kaplama hücresinin;
- Anot kutbunda: Gümüş elektrot yükseltgenir ve Ag+ iyonuna dönüşür.
- Ag → Ag+ + e–
- Katot kutbunda: Çözeltideki Ag+ iyonları indirgenir ve Ag metali olarak kaşığın yüzeyini kaplar.
- Ag+ + e– → Ag
Katodik Koruma

- Paslanmasını istemediğimiz bir metale, daha aktif bir metal bağlarsak, paslanmasının önüne geçmiş oluruz.
- Çünkü, paslanmada, aktif metalin önceliği vardır.
- Çünkü; elektron verme eğilimi daha yüksek olan metal önce yükseltgenir.
- Bir metali korumak için, o metale bağlana daha aktif metale, “kurban elektrot” denir.
- Kurban elektrot olarak görev yapan metal anot görevi yapar ve diğer metalin paslanmasının önüne geçer.
- Paslanmasını engellediğimiz metal de katot görevi yapar. Bu yüzden bu yöntem, “katodik koruma” adını alır.
Katodik koruma yönteminin bazı uygulamaları şunlardır:
- Boru hatlarındaki metal boruların korozyonunu önleme
- Gemilerin gövdelerinin korozyonunu önleme
- Metal tankların, havuzların korozyonunu önleme


Elif says:
Teşekkürler hocam çok iyi bir konu anlatımı olmuş.🙂