İçindekiler
- Sıvılar, katıların erimesiyle oluşan maddelerdir.
- Sıvılar aşağıdaki özellikleri taşırlar:
- Kimyasal türler katıdan daha düzensizdir.
- Kimyasal türler arası boşluk katılara göre daha fazladır.
- Yoğunluğu katıdan daha az, gazdan daha çoktur.
- Kimyasal türler titreşim ve öteleme hareketi yapar.
- Sıkıştırılamazlar.
- Akışkandırlar.
- Belli bir hacimleri vardır fakat; kaplarının şekillerini alırlar.
Aşağıdaki vidyoda, sıvı haldeki su moleküllerinin hareketi canlandırılmıştır:
Sıvıların Temel Özellikleri
- Sıvılar, katılar gibi çeşitli sınıflara ayrılmaz.
- Bütün sıvıların belli temel özellikleri vardır. Bu özellikleri bilmek, sıvıları tanımak için yeterlidir.
- Sıvıların temel özellikleri şunlardır:
- Viskozite
- Buharlaşma ve Denge Buhar Basıncı
- Kaynama
1. Viskozite
- Sıvıların akmaya karşı gösterdikleri dirence viskozite denir.
- Viskozitenin zıttı akışkanlıktır.
- Bir sıvının akışkanlığı arttıkça viskozitesi azalır, viskozitesi arttıkça akışkanlığı azalır.
- Bal ve su, hepimizin mutlaka gördüğü sıvılardır.
- Akışkanlık açısından bakarsak, su daha akışkandır, balın akışkanlığı sudan düşüktür.
- Viskozite açısından bakarsak, bal daha viskozdur, suyun viskozitesi baldan düşüktür.
Viskozite ölçülürken sıvılar aynı açıyla akıtılır:
Aşağıdaki resimde, farklı viskozitedeki sıvılar ile yapılan bir akışkanlık deneyi verilmiştir:

Motor yağları ile viskozite deneyini izle:
Viskozite arttıkça batma süresi de artar:
- Viskoz sıvılar, viskozitesi yüksek sıvılardır.
- Viskozite arttıkça, katılar sıvının dibine yavaş batar.
- Akıcılık arttıkça, katı sıvının dibine hızlı batar.
- Yandaki videonun ilk 15 saniyesi bu olayın deneyidir:
Viskoziteyi Etkileyen Faktörler
- Viskozite, şu faktörlerden etkilenir:
- Moleküller Arası Çekim Kuvvetleri (Zayıf etkileşimler)
- Sıcaklık
I) Moleküller Arası Çekim Kuvvetleri (Zayıf etkileşimler)
- Moleküller arası etkileşimlerin (zayıf etkileşimlerin) kuvveti arttıkça, sıvıların viskozitesi artar, akışkanlığı azalır.
- Molekül ağırlığı arttıkça genellikle zayıf etkileşimler de güçlenir, viskozite artar.
- Gliserin molekülleri arasına üçer tane Hidrojen bağı kurulurken, su molekülleri arasına birer tane Hidrojen bağı kurulur.
- Bu yüzden Gliserin moleküllerinin birbirinden koparak akmaları sudan daha zordur, viskoziteleri sudan daha yüksek, akışkanlıkları daha düşüktür.

II) Sıcaklık
- Sıcaklık arttıkça akışkanlık artar, viskozite azalır.
- Sıcak bal daha akışkandır, sıcak reçel daha akışkandır. Sıcaklık arttıkça, moleküller arası etkileşimler zayıflar, akma olayı kolaylaşır.

Örnek:
I) 20oC’de bal
II) 20oC’de su
III) 40oC’de su
Yukarıda verilen maddelerin viskoziteleri arasındaki ilişki hangi seçenekte doğru olarak verilmiştir?
A) I>II>III
B) I>III>II
C) III>I>II
D) III>II>I
E) II>III>I
Sorunun Doğru Cevabı
Sorunun Çözümü
2. Buharlaşma
- Sıvının yüzeyindeki moleküllerin, buhar haline geçmesine buharlaşma denir.
- Tıpkı sıvılar gibi, bazı katılar da buharlaşır (süblimleşme).
- Böyle katılara uçucu katılar denir.
- Buharlaşma olayı sadece yüzeydeki sıvı molekülleri tarafından gerçekleştirilir.

- Buharlaşma olayı, ısı alan (endotermik) bir olaydır.
- Bu yüzden, bir karpuzun kabuğundaki su buharlaşırken karpuz soğur.
- Bu yüzden, denizden çıktığımızda, cildimizdeki su buharlaşırken üşürüz.
Buharlaşma Hızı
- Birim zamanda buharlaşan molekül sayısına buharlaşma hızı denir.
- Buharlaşma hızı yüksek olan sıvılar uçucu sıvalar olarak adlandırılır.
- Sıvıların buharlaşma hızları farklı farklıdır.
Buharlaşma Hızına Etki Eden Faktörler
I) Maddenin Cinsi (Kaynama Noktası)
- Kaynama noktası daha yüksek olan sıvının:
- Buharlaşma hızı düşüktür.
- Zayıf etkileşimlerin kuvveti daha fazladır.
- Kaynama noktası daha düşük olan sıvılar daha hızlı buharlaşır.
II) Yüzey Alanı
- Sıvının yüzey alanı arttıkça, buharlaşma hızı da artar.
- Çünkü; buharlaşma sıvının yüzeyinden gerçekleşen bir olaydır.
- Geniş ağızlı kaplardaki su daha hızlı buharlaşır, dar ağızlı kaplardaki su daha yavaş buharlaşır.
III) Sıcaklık
- Bir sıvının sıcaklığı arttıkça buharlaşma hızı da artar.
- Sıcaklık, kaynama noktasına geldiğinde, buharlaşma hızı maksimum değerine ulaşır.
- Kaynayan sıvılar, sadece yüzeyinden değil her bölgesinden buharlaşır.
IV) Nem ve Rüzgar
- Havadaki nem arttıkça, buharlaşma hızı azalır.
- Nemli havalarda, çamaşırlarımız daha uzun sürede kurur, kuru havalarda daha çabuk kurur.
- Rüzgar, buharlaşma hızını arttırır.
- Rüzgarlı havalarda, çamaşırlarımız daha kısa sürede kurur.
Örnek:
Yıkanan bir çamaşırın kuruması için, emdiği suyun buharlaşması gerekir.
Buna göre, ıslak bir çamaşırın daha hızlı kuruması için;
I) Katlayarak asmak
II) Gölgeye değil güneşin altına asmak
III) Rüzgarlı yerlerden uzak tutmak
işlemlerinden hangisini yapmak işe yarayacaktır?
A) Yalnız I
B) Yalnız II
C) Yalnız III
D) I ve II
E) I, II ve III
Sorunun Doğru Cevabı
Sorunun Çözümü
Denge Buhar Basıncı (Pbuhar)
- Her buharın (gazın), mutlaka bir basıncı olur.
- Denge buhar basıncı, bir sıvının buharının yaptığı basınçtır.
- Sıvılar her sıcaklıkta buharlaşma yeteneğine sahiptir.
- Bir sıvının buharlaşması için ısıtılmasına gerek yoktur.
- Sıvıların soğutulması buharlaşma olayını yavaşlatır fakat durdurmaz.
- Yıkanan çamaşırlarımızın, yaz-kış kurumalarının sebebi tam olarak budur.
Denge Buhar Basıncı Nasıl Hesaplanır?
- Sıvı kapalı bir kaba konulur ve kabın ağzı kapatılır. (Sıvının sıcaklığı da sabitlenir.)
- Kabın içinde, gözümüzle göremesek de şu olaylar gerçekleşir:
- Sıvının yüzeyindeki kimyasal türler (moleküller), her zaman yaptıkları gibi buharlaşmaya devam ederler.
- Kapak kapalı olduğundan, sıvının üzerinde buhar birikmeye başlar.
- Bir süre sonra, buharlaşan kimyasal türlerden bazıları, tekrar sıvı hale dönmeye başlar, yani yoğunlaşma başlar.
- Yani, hem buharlaşma hem de yoğunlaşma tepkimeleri aynı anda gerçekleşir.
- Sıvı eğer su olsaydı, bu iki tepkime şöyle gösterilirdi:
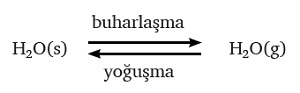
- Başlangıçta buharlaşma hızı, daha fazladır. Fakat; buhar miktarı arttıkça, buharlaşma yavaşlar, yoğunlaşma hızlanır.
- Bir süre sonra, buharlaşma hızı ile yoğunlaşma hızı birbirine eşitlenir.
- İşte bu eşitliğin kurulduğu andan sonra, sıvının üzerindeki buhar miktarı da sıvı miktarı da artık değişmez.
- Çünkü; kaç tane sıvı molekülü buhar haline geçiyorsa o kadar buhar molekülü de sıvı hale geçiyordur.
- Buharlaşma ve yoğunlaşma hızının eşitlendiği anda, artık, sıvı-buhar dengesi kurulmuş demektir.

- Grafikte:
- Vbuh : buharlaşma hızı
- Vyoğ : yoğuşma hızı
- t: Buharlaşma ve yoğunlaşma hızlarının eşitlendiği andır.
- Sıvı-buhar dengesi kurulduktan sonra, buharın yaptığı basınca denge buhar basıncı veya buhar basıncı denir.
Buhar basıncı animasyonu:
- Aşağıda/yanda, kapalı bir kapta, sıvı-buhar dengesini kurmuş brom sıvısı (Br2(s)) verilmiştir.
- Dikkat edilirse, buharlaşma ve yoğunlaşma olayları sürekli devem etmektedir.
- Fakat, buhar halindeki ve sıvı haldeki moleküllerinin sayısı hep aynı kalmaktadır.
- Tabi gerçekte, denge anında çok daha fazla buhar molekülü bulunur.
Denge Buhar Basıncı Nelere Bağlıdır?
I) Sıvının Cinsine – Kaynama Noktasına
- Her sıvının bir kaynama noktası vardır.
- Aynı ortamdaki sıvılardan, kaynama noktası daha küçük olan sıvının, denge buhar basıncı daha büyüktür.
- Kaynama noktası yüksek olan sıvılarda, kimyasal türler, birbirine daha kuvvetli bağlı demektir.
- Bu yüzden kaynama noktası yüksek olan sıvıların buharlaşması zor olur.
II) Sıcaklığa
- Bir sıvının sıcaklığı arttıkça, buhar basıncı da artar.
- Açık havada ve kaynama sıcaklığına geldiğinde, sıvının buhar basıncı, atmosfer basıncına eşitlenir.
III) Safsızlığa
- Safsızlık, bir sıvıda başka bir maddenin çözünmesi ile oluşur.
- Sıvıda çözünen madde, sıvıdan daha uçucu ise, sıvının buhar basıncı artar.
- Sıvıda çözünen madde, uçucu bir madde değilse, sıvının buhar basıncı azalır.
- Tuzlar, uçucu olmayan katılardır.
- Suda tuz çözersek, suyun denge buhar basıncı düşer.
Örnek:
| ___Sıvı___| | ___Buhar Basıncı (mmHg)___ |
| X | 400 |
| Y | 80 |
| Z | 120 |
Yukarıdaki tabloda, saf X, Y ve Z sıvılarının, aynı ortamdaki buhar basınçları verilmiştir.
Buna göre bu sıvılar için;
I) Kimyasal türleri arasındaki etkileşimi en güçlü olan Y sıvısıdır.
II) Kaynama noktası en düşük olan X sıvısıdır.
III) X sıvısının buharlaşma hızı Z sıvısından daha büyüktür.
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız II
C) Yalnız III
D) I ve II
E) I, II ve III
Sorunun Doğru Cevabı
Sorunun Çözümü
Kaynama Olayı
- Sıvılar, buhar basınçları ile atmosfer basıncının eşitlendiği sıcaklıkta kaynarlar.
- Kaynayan bir sıvının:
- Sıcaklığı kaynama sıcaklığındadır.
- Buhar basıncı, atmosfer basıncına eşittir.
Açık Hava Basıncı (Pdış)
- Açık hava bir gaz karışımıdır.
- Bu yüzden, her gazın olduğu gibi açık havanın da bir basıncı vardır.
- Açık hava basıncına “atmosfer basıncı” ya da “dış basınç” da denir.
- Açık hava basıncının sembollü olarak aşağıdakilerden herhangi biri kullanılabilir:
- P0 veya Pdış veya Patm veya Phava
Kaynama Şartı
- Kaynamayan sıvıların buhar basınçları, her zaman, dış basınçtan daha küçüktür.
- Sıvılar ısıtıldıkça sıcaklıkları artar.
- Sıcaklıkları arttıkça, buhar basınçları (Pbuhar) artar.
- Hangi sıcaklığa geldiğinde, sıvının buhar basıncı, üzerindeki atmosferin basıncına (Pdış) eşitlenir, o sıcaklıkta sıvı kaynar.
- Yani bir sıvı kaynıyorsa aşağıdaki eşitlik kurulmuş demektir:
Pbuhar = Pdış
- Kaynamayan bir sıvıda, buharlaşma, sadece sıvının yüzeyinde olur fakat kaynayan bir sıvı, her yerinden buharlaşır.
- Saf bir sıvı, sabit dış basınç altında kaynarken, sıcaklığı, kaynama olayının başından sonuna kadar sabit kalır.
Normal Kaynama Noktası
- Normal kaynama noktası, normal koşullardaki kaynama sıcaklığıdır.
- Normal koşullar, hava basıncının “1 atm” yani 1 atmosfer olduğu her yerdir.
- Normal koşullarda sıcaklık da 25oC olur.
- Mesela, saf su, normal koşullarda, 100 oC’ye geldiğinde, buhar basıncı 1 atm olur ve kaynamaya başlar.
- Bu yüzden saf suyun normal kaynama sıcaklığı 100 oC’dir.
Kaynama Sıcaklığına Etki Eden Faktörler
I) Sıvının Cinsi – Zayıf Etkileşimler
- Her saf sıvının belli ve sabit bir kaynama sıcaklığı vardır.
- Sıvıların kaynama sıcaklığı, kimyasal türleri arasındaki zayıf etkileşimlere bağlıdır.
- Daha sağlam zayıf etkileşimler kuran sıvıların, kaynama sıcaklığı daha yüksek olur.
II) Dış Basınç
- Sıvının üzerindeki gaz ister açık hava olsun, ister başka bir gaz olsun, sıvının kaynama sıcaklığına doğrudan etki eder.
- Sıvıların üzerindeki dış basınç arttıkça kaynama noktaları da yükselir; dış basınç düştükçe de kaynama sıcaklığı düşer.
- Mesela; dağlara tırmandıkça hava basıncı azalır ve dağların tepelerinde sıvılar daha düşük sıcaklıkta kaynar. Everest tepesi, dünyanın en yüksek tepesidir ve burada saf su, 78 oC’de kaynar.
III) Safsızlık
- Sıvının içinde, yemek tuzu gibi, uçucu olmayan bir katı çözersek, sıvının kaynama noktası yükselir, donma noktası da düşer.
- Sıvının; az ya da çok olması, kabın şekli, ısıtıcının gücü sıvıların kaynama sıcaklığına etki etmez.
Örnek:
Bir sıvının, kimyasal türleri arasındaki zayıf etkileşimlerin cinsi ve kuvveti, sıvının;
I) Viskozite
II) Kaynama ve donma sıcaklığı
III) Buhar basıncı
IV) Buharlaşma hızı
özelliklerinden hangilerini doğrudan etkiler?
A) I ve II
B) I ve II
C) II, III ve IV
D) I, III ve IV
E) I, II, III, IV
Sorunun Doğru Cevabı
Sorunun Çözümü
Kaynama VS Buharlaşma
Buharlaşma olayı:
- Sıvılar her sıcaklıkta mutlaka buharlaşırlar.
- Buharlaşma olayı, sıvının sadece yüzeyinde gerçekleşir.
- Buharlaşma daha yavaştır.
- Kabarcık oluşmaz.
- Az enerji gerektirir.
Kaynama olayı:
- Sadece kaynama sıcaklığında gerçekleşir.
- Sıvı, her yerinden buharlaşır.
- Buharlaşma hızının maksimum olduğu zamandır.
- Sıvının her yerinden kabarcıklar çıkar.
- Çok enerji gerektirir.
Atmosferde Su Buharı
- Sıvılar her sıcaklıkta buharlaştığı için yeryüzündeki sular da, buharlaşarak havaya karışır.
- Bu yüzden, solduğumuz havada az yada çok miktarda su buharı vardır.
Nem (Mutlak Nem)
- Havada bulunan su buharı miktarına nem veya mutlak nem denir.
- Havanın sıcaklığı arttıkça yeryüzünde buharlaşma arttığı için, nem miktarı da artar.
- Yaz aylarında ve özellikle Akdeniz kıyılarında nem oranının yükseldiğini biliriz.
- Su buharı bulunmayan havaya kuru hava denir.
- Nemli hava ise su buharı ve kuru havanın bulunduğu karışımdır.
Bağıl Nem
- Havanın taşıyabileceği maksimum bir nem oranı vardır.
- Hava kütlesinin taşıyabileceği en fazla nem miktarına havanın o sıcaklıktaki doygunluk noktası denir.
- Doygunluk noktasına gelen hava, daha fazla nem alamayacağı için, sıcaklık düştüğü zaman yağış başlar.
- Havanın neme doyup doymadığını ifade etmek için, bağıl nem kavramı kullanılır.
- Bağıl nem; belli bir sıcaklıkta havada bulunan su buharı miktarının, havanın o sıcaklıkta taşıyabileceği en fazla su buharı miktarına oranıdır.
- Bağıl nem 1 m3 havanın neme doyma oranı olarak da tanımlanabilir.
- Bağıl nem % 100 olduğunda, havadaki nem miktarı maksimum seviyeye ulaşmış demektir.
Gölgede, Gerçek ve Hissedilen Sıcaklık
- Gölgede sıcaklık dış ortam şartlarından (Güneş ışığı, rüzgar, yağış vb. ) arındırılmış ortamda ölçülen sıcaklık değeridir.
- Bir bölgede, termometre ile ölçülen sıcaklık “gerçek sıcaklık” tır.
- Ancak bir sıcaklığın ölçüldüğü yerdeki bağıl nem oranı ve rüzgâr etkisi bu sıcaklığın canlılar tarafından farklı algılanmasına sebep olur.
- Ölçülen değil, vücudumuz tarafından algılanan sıcaklıktan, hissedilen sıcaklık olarak bahsedilir.
- Genellikle bağıl nem arttıkça hissedilen sıcaklık artar.
- Rüzgâr arttıkça serinletme etkisinden dolayı hissedilen sıcaklık azalır.
- Örneğin gerçek sıcaklığın 35 °C olduğu bir bölgede:
- Bağıl nem %60 ise hissedilen sıcaklık 45 °C olur.
- Bağıl nem %5 ise hissedilen sıcaklık 32 °C olur.
- Hazırlanmış çizelgeler yardımı ile ölçülen sıcaklık, bağıl neme bağlı olarak hissedilen sıcaklığa çevrilebilir.

2 yorum “3. Sıvılar”