Maddenin Halleri → 4. Bölüm
Gazlar
Dersin Özellikleri:
- Seviye: Hiç Bilmeyenler İçin
- Süre: 40 dakika
- Gerekli Bilgiler:
- Kimyasal Türler Arası Etkileşimler
- Öğretmen:
- Gökalp AY
Anlatılacak Başlıklar*:
- Gazlar
- Gazların Genel Özellikleri
- Gazları Tanımlayan Özellikler
- Saf Maddelerin Hal Değişim Grafikleri
* Konu anlatımı, örneklerle zenginleştirilmiştir.
Gazlar
Gazların Genel Özellikleri
- Sıvıların kaynaması veya buharlaşması ile oluşurlar.
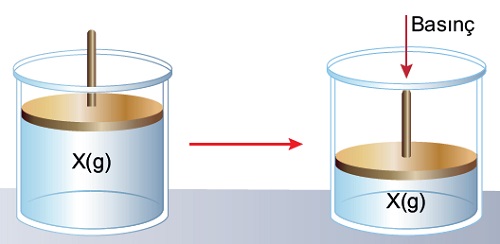
- Kapların hacmini ve şeklini alırlar.
- Sıkıştırılabilirler.
- Her zaman homojen karışırlar.
- En düşük öz kütleli halidir.
- Kimyasal türleri arasında bir etkileşim yok kabul edilir.
- Kimyasal türleri; titreşim, öteleme ve dönme hareketi yaparlar.
- Maddenin en düzensiz hâlidir.
- Akışkandırlar.
- Enerjisi en yüksek halidir.
- Kaplarına basınç uygularlar.
Gazlar
Gazları Tanımlayan Özellikler
- Bir gazı tarif ederken şu özellikleri kullanılır:
- Basınç (P)
- Miktar
- Hacim (V)
- Sıcaklık (T)
1. Basınç (P)
- Birim yüzeye uygulanan kuvvete basınç denir.
- Basıncın sembolü P harfidir; birimi atm (atmosfer) veya mmHg (milimetre cıva)’dır.
- Gazların kaplarına uyguladığı basınca gaz basıncı denir.
- Gazlar, kabın her yerine eşit basınç uygularlar.
Suyun Gaz Hali
- Hava da bir gaz karışımıdır ve bir basıncı vardır.
- Havanın basıncına “açık hava basıncı” veya “atmosfer basıncı” denir.
- Atmosfer basıncı “P0” veya “Phava” sembolü ile ifade edilir.
- Torricelli, normal koşullarda açık hava basıncı 760 mmHg hesaplamıştır.
1 atm = 760 mmHg
1 atm = 76 cmHg
Gazlar
Gazları Tanımlayan Özellikler
2. Miktar
- Gazların miktarı genellikle mol sayısı olarak ifade edilir.
- Mol sayısının sembolü “n” harfidir, birimi de “mol” dür.
- 1 mol gazın kimyasal türleri, Avogadro Sayısı kadardır.
Avogadro Sayısı = NA = 6,02×1023
- 1 mol He (Helyum) gazında, 6,02×1023 tane He atomu vardır.
- 1 mol N2 (Azot) gazında, 6,02×1023 tane N2 molekülü vardır.
- 1 mol NH3 (Amonyak) gazında, 6,02×1023 tane NH3 molekülü vardır.
Gazlar
Gazları Tanımlayan Özellikler
3. Hacim (V)
- Bir maddenin, boşlukta kapladığı yere hacim denir.
- Hacmin sembolü V harfidir; birimi Litre (L) veya m3 tür.
- Gazların hacimleri, kaplarına bağlıdır.
- Kabının hacmi kaç litre geliyorsa, gazın da hacmi o kadardır.
- Hacmin birimi Litredir (L).
1L = 1 dm3 = 1000 mL = 1000 cm3
- Belli koşullarda, belli miktardaki gazların hacimlerini ezbere bilmekte fayda vardır:
- Standart koşullar: Basıncı 1 atm, sıcaklığı 25 oC olan gazlar standart koşullarda kabul edilir. Oda koşulları da denir.
- Standart koşullarda, 1 mol gaz, her zaman, 24,5 L hacim kaplar
- Normal koşullar: Basıncı 1 atm, sıcaklığı 0 oC olan gazlar normal koşullarda kabul edilir.
- Normal koşullarda, 1 mol gaz, her zaman, 22,4 L hacim kaplar.
- Standart koşullar: Basıncı 1 atm, sıcaklığı 25 oC olan gazlar standart koşullarda kabul edilir. Oda koşulları da denir.
Gazlar
Gazları Tanımlayan Özellikler
4. Sıcaklık (T)
- Sıcaklık termometre ile ölçülür.
- Kelvin cinsinden sıcaklığa mutlak sıcaklık denir ve T harfi ile gösterilir.
- Celsius (oC) cinsinden sıcaklık, bizim, günlük hayatta kullandığımız sıcaklıktır ve t harfi ile gösterilir.
Kelvin (K) = Celcius (oC) + 273
veya
T = t + 273
- Sıcaklık, doğrudan, kimyasal türlerin hızı ile ilgilidir.
- Bir gaz veya bir madde ne kadar sıcaksa, kimyasal türleri de o kadar hızlıdır.
- Bir madde ne kadar sıcaksa, maddedeki kimyasal türlerin ortalama kinetik enerjisi o kadar fazladır.
- Sıcaklıkları eşit olan maddelerde, kimyasal türlerin, ortalama kinetik enerjileri de eşittir.
Gazlar
Saf Maddelerin Hal Değişim Grafiği
Isıtılan saf bir katının sıcaklık-zaman grafiği:
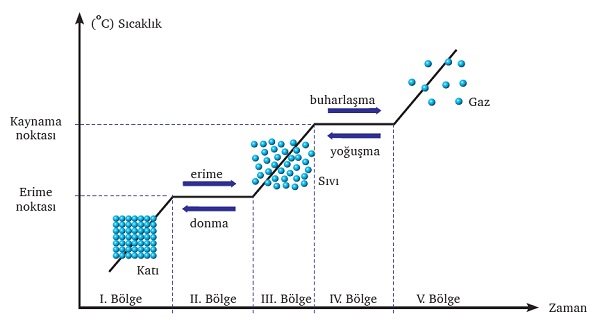
I. Bölge:
- Madde katıdır.
- Isıtıldıkça sıcaklığı artar.
- Maddenin ortalama kinetik enerjisi artarak titreşim hareketleri hızlanır.
- Madde homojendir.
II. Bölge:
- Madde erimektedir.
- Sıcaklık erime süresince sabittir.
- Madde heterojendir.
III. Bölge:
- Madde sıvıdır.
- Sıcaklık ve ortalama kinetik enerji arar.
- Madde homojendir.
Gazlar
Saf Maddelerin Hal Değişim Grafiği
Isıtılan saf bir katının sıcaklık-zaman grafiği:

IV. Bölge:
- Madde kaynama sıcaklığındadır.
- Madde kaynar.
- Sıcaklık kaynama süresince sabittir.
- Bu bölgede sıvı-gaz bir arada bulunur, madde heterojendir.
V. Bölge:
- Madde buhar halindedir.
- Verilen ısı, gazın sıcaklığını yükseltir.
- Bu bölgede madde homojendir.
Gazlar
Saf Maddelerin Hal Değişim Grafiği
Soğutulan saf bir gazın sıcaklık-zaman grafiği:
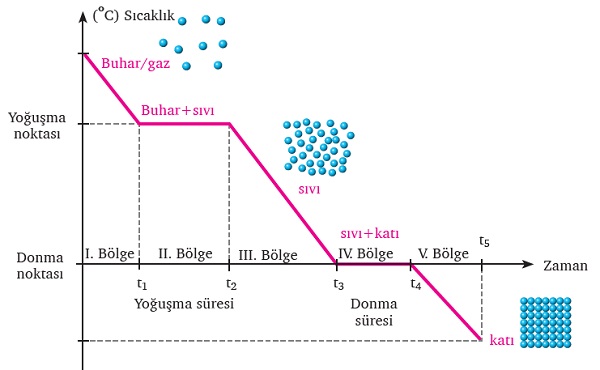
I. Bölge:
- Madde gazdır.
- Sıcaklık ve ortalama kinetik enerji düşer.
- Madde homojendir.
II. Bölge
- Madde sıvı-buhar halindedir, heterojendir.
- Sıcaklık sabit ve yoğunlaşma sıcaklığıdır.
III. Bölge:
- Madde sıvı halindedir.
- Sıcaklık ve ortalama kinetik enerji düşer.
- Bu bölgede madde homojendir.
Gazlar
Saf Maddelerin Hal Değişim Grafiği
Soğutulan saf bir gazın sıcaklık-zaman grafiği:

IV. Bölge:
- Madde donma sıcaklığındadır.
- Sıcaklık sabittir.
- Katı-Sıvı haldedir.
- Heterojendir.
V. Bölge:
- Madde katı halindedir.
- Sıcaklığı ve ortalama kinetik enerjisi düşer..
- Bu bölgede madde homojendir.

Maddenin Halleri
IV. Bölüm
(Gazlar)
Bitti 🙁