Dalton Atom Modeli’nde yer alan,
I) Atom parçalanamaz.
II) Atomlar, içi dolu küreciklerdir.
III) Kimyasal tepkimelerde atomların cinsi ve sayısı değişmez.
IV) Bir elementin bütün atomları özdeştir.
yargılarından hangileri günümüzde de geçerlidir?
İçindekiler
DERS
TYT Kimya
Kimya 9
KONU
ÜNİTE II
ATOM ve Periyodik Sistem
I. Bölüm
Atom ve Periyodik Sistem
Bu ünitenin 3 bölümü vardır:
1- Atom Modelleri
2- Atomun Yapısı
3- Periyodik Sistem
TYT Sınavında
“Atom ve Periyodik Sistem”
Sorularının Sayıları
| Yıl | 2025 | 2024 | 2023 | 2022 | 2021 | 2020 | 2019 | 2018 |
| Soru Sayısı | 1 | 1 | 1 | 1 | 1 | 1 | 2 | 1 |
Dersin Özellikleri:
Anlatılacak Başlıklar*:
* Konu anlatımı, örneklerle zenginleştirilmiştir.

Bu model; kimyanın temel kanunları ile çelişmez.
Dalton Atom Modeli’nde yer alan,
I) Atom parçalanamaz.
II) Atomlar, içi dolu küreciklerdir.
III) Kimyasal tepkimelerde atomların cinsi ve sayısı değişmez.
IV) Bir elementin bütün atomları özdeştir.
yargılarından hangileri günümüzde de geçerlidir?
Yalnız III
I ve II
III ve IV
II ve IV
I, III ve IV
Dalton Atom Modeli’nde aşağıdaki ifadelerden hangisi yer almaz?
Bütün maddeler atom adı verilen küreciklerden oluşur.
Atomlarda, pozitif yüke eşit miktarda negatif yük vardır.
Farklı elementlerin atomları da farklıdır.
Atomlar sabit oranlarda birleşerek bileşikleri oluştururlar.
Atom parçalanamaz.
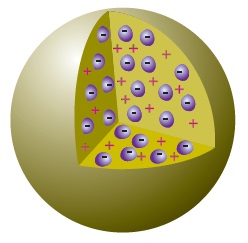

Thomson Atom Modeli’inde,
I) Atomda pozitif ve negatif yükler vardır.
II) Negatif yüklü elektronlar, çekirdek etrafındaki yörüngelerde bulunur.
III) Üzümlü kekteki üzüm ve kek hamuru gibi, negatif ve pozitif yükler, atomda homojen olarak dağılmışlardır.
IV) Atomlar nötr yapıdadır.
ifadelerinden hangisi her almaz?
Yalnız I
Yalnız II
I ve IV
II, III ve IV
I, III ve IV
Aşağıda verilen bilgilerden hangisi, diğerlerinden sonra ortaya atılmıştır.
Bütün maddeler atom adı verilen küreciklerden oluşur.
Atomlar, çapı yaklaşık 10-8 cm olan küreciklerdir.
Farklı elementlerin atomları da farklıdır.
Atomlar sabit oranlarda birleşerek bileşikleri oluştururlar.
Atom parçalanamaz.

Rutherford Atom Modeli’inde yer alan,
I) Atomda pozitif yük miktarı negatif yük miktarına eşittir.
II) Pozitif yükler, atomun çekirdeğinde toplanmıştır.
III) Pozitif yüklerin kütlesi, atomun kütlesinin yaklaşık yarısıdır.
ifadelerinden hangisi Thomson Atom Modeli’nde yer almaz?
Yalnız I
Yalnız II
Yalnız III
II ve III
I, II ve III
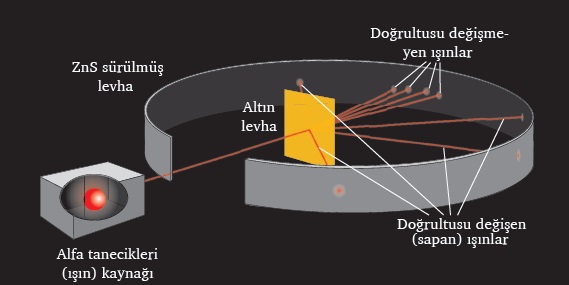
Rutherford, yaptığı deney ile altın atomlarının üzerine alfa ışınları göndermiş ve sonuçlarını değerlendirerek, bir atom modeli ortaya atmıştır.
Bu deney ile ilgili olarak aşağıdakilerden hangisi doğru değildir?
Deney sonucunda atomun çekirdeği keşfedilmiştir.
Deney, Thomson Atom Modeli’ni test etmek için yapılmıştır.
Elektronların çekirdek etrafında bulunduğu keşfedilmiştir.
Atomun büyük boşluklara sahip olduğu anlaşılmıştır.
Nötronlar keşfedilmiştir.



Atomların oluşturduğu spektrumlar ile ilgili olarak aşağıda verilen ifadelerden hangisi doğru değildir?
Güneş ışığı, prizmadan geçirildiğinde sürekli spektrum elde edilir.
Gaz halindeki bir elementin ısıtılması sonucu emisyon (ışıma) spektrumu elde edilir.
Bütün atomların spektrumları aynıdır.
Absorbsiyon ve emisyon spektrumları bir birinin tam tersidir.
Çizgi spektrumlarında karanlık ve aydınlık bölgeler bulunur.
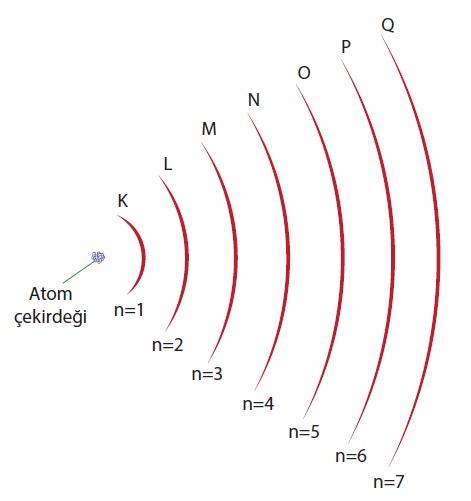
Bohr Atom Modeli hakkında verilen bilgilerden hangisi doğru değildir?
Elektronlar çekirdek etrafında ve belirli yörüngelerde bulunur.
Enerjisi en düşük elektronlar K kabuğunda bulunur.
Temel haldeki atom, enerjisi en düşük olan atomdur.
Enerji alan atom, uyarılmış hale geçer.
Elektronlar, bulundukları yörüngeleri asla terk etmezler.

Atom ve Periyodik Sistem
I. Bölüm
(Atom Modelleri)
Bitti 🙁