İçindekiler
- Organik bileşiklerin sınıflandırılmasında bu bileşiklerin “fonksiyonel grupları” dikkate alınır.
- Tanım olarak; organik moleküllerin, kimyasal tepkimelere girme eğilimlerini ve bazı fiziksel özelliklerini belirleyen atom gruplarına “fonksiyonel gruplar” denir.
- Fonksiyonel gruplar; organik moleküllerin diğer kısımlarından farklı olan atom gruplarıdır.
- Bir organik bileşiğin, ne tür bir organik bileşik olduğu, fonksiyonel grubuna bakara anlaşılır.
Aşağıda, bizi ilgilendiren organik bileşik sınıfları ve fonksiyonel grupları verilmiştir:

Bu bir reklamdır:
Alkoller
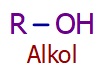
- Alkollerin fonksiyonel grubu -OH (hidroksil) grubudur.
- Alkollerin genel formülü CnH2n+2O şeklindedir.
- Bir alkan molekülünde, bir H atomunu koparıp, yerine OH bağlarsak, bir alkol molekülü elde ederiz.
- Alkoller, su (H-OH) molekülündeki bir H atomunun yerine alkil (R-) gurubunun bağlanması ile de oluşur. Bu yüzden alkollere, “alkillenmiş su” da denilir.
Aşağıda bazı alkol molekülleri verilmiştir:

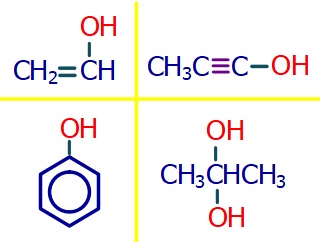
- -OH grubu şu şartları taşıyorsa bileşik bir alkol değildir;
- İkili ya da üçlü bağ yapmış bir karbon atomuna bağlı ise
- Fenil grubuna bağlanmış ise
- Aynı karbon atomunda iki tane ise
Aşağıda verilen bileşikler alkol değildir:
Bu bir reklamdır:
Alkollerin Adlandırılması
IUPAC sistemine göre, alkolleri adlandırırken şu kurallara uyulur:
- İçinde -OH grubunun da bulunduğu en uzun karbon zinciri bulunur. Bu zincir, bileşiğin gövdesi olur.
- Gövdeye bağlı diğer gruplar dallardır.
- Önce numaraları ile birlikte dallar okunur, sonra -OH grubunun yerini de belirterek gövde okunur.
- Alkol grubunun gövdesi, karbon sayısı kadar alkanın adının sonunda “-ol” son eki getirilerek okunur.
- Alkollerin, yaygın isimlerinde, -OH grubunun bağlı olduğu alkil grubunun adına ve “alkol” kelimesi eklenir.
Öğretici Örnek:
1 ve 2 karbonlu alkollerde, -OH grubunun numarasına gerek yoktur:

Bu bir reklamdır:
Öğretici Örnek:
Numara vermeye -OH grubuna yakın uçtan başlanır: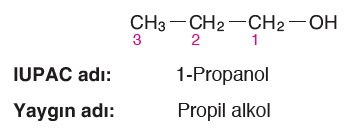
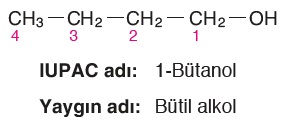
Bu bir reklamdır:
Öretici Örnek:
Gövdenin isminden önce -OH grubunun bağlı olduğu karbon atomunun numarası da belirtilir: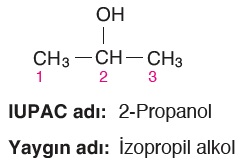

Bu bir reklamdır:
Öğretici Örnek:
Önce dalların numarası ve adı sonra da -OH grubunun numarası ve gövdenin adı okunur:
Bu bir reklamdır:
Öğretici Örnek:
Dalların ve -OH grubunun numarası belitilir:
Bu bir reklamdır:
Öğretici Örnek:
Aromatik alkoller de vardır:
Bu bir reklamdır:
Öğretici Örnek:
Alkenlerden türemiş alkoller de vardır:
Bu bir reklamdır:
Öğretici Örnek:
Alkinlerden türemiş alkoller de vardır: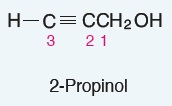
Bu bir reklamdır:
Öğretici Örnek:
Siklo alkoller de vardır: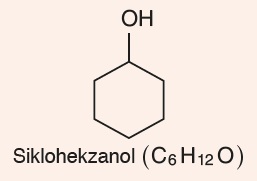
Mono ve Poli Alkoller
- Bir alkol molekülünde 1 tane -OH grubu varsa, bu alkol molekülü, mono alkol olarak adlandırılır.
Öğretici Örnek:
Aşağıda; mono alkollere örnekler verilmiştir:
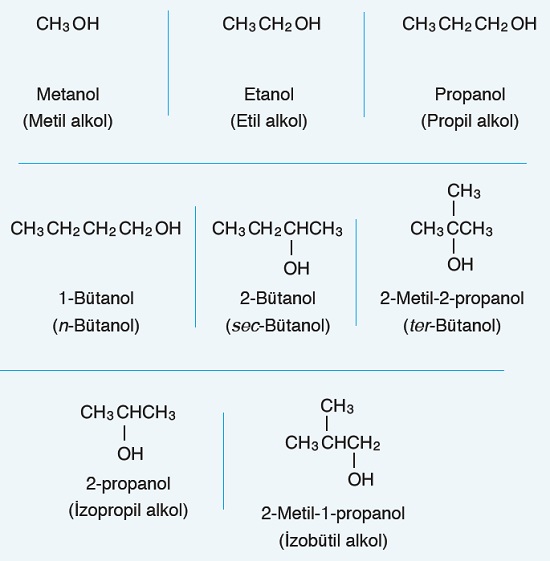
- Bir alkol molekülünde, birden çok -OH grubu varsa bu alkol molekülü, polialkol olarak adlandırılır.
- Bir polialkolde, iki tane -OH grubu varsa dialkol, üç tane -OH grubu varda trialkol olarak sınıflandırılabilir.
Öğretici Örnek:
Aşağıda polialkollere örnekler verilmiştir:

Bu bir reklamdır:
Etandiol Ve Gliserin
- Etandiol, bazı polimerlerin üretiminde ham madde olarak kullanılır.
- Etandiol, donmayı önleyici (antifriz) bir maddedir; ancak zehirli bir madde olmasından dolayı; araç motorlarında antifriz olarak propilen glikol (1,2-propandiol)
- Gliserin, tatlandırıcı madde olarak gıda endüstrisinde kullanılmaktadır. Ağız bakım suyu, nemlendirici krem gibi kişisel bakım ürünlerinin, şurupların ve bazı ilaçların yapısında gliserin vardır.
- Ayrıca gliserin, bazı patlayıcıların üretiminde (nitro gliserin) ham madde olarak önemli bir yere sahiptir.
Primer – Sekonder – Tersiyer Alkoller
- Alkollerde hidroksilin bağlı olduğu karbon atomu, α (alfa) karbon atomu olarak ifade edilir.
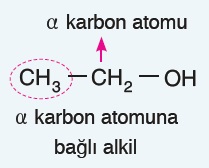
- Alkol molekülünde, -OH grubunun bağlı olduğu C atomuna 1 tane C atomu bağlı ise; o alkol birincil veya primer (1o) alkol olarak sınıflandırılır. (CH3OH de birincil alkoldür.)
- Alkol molekülünde, -OH grubunun bağlı olduğu C atomuna 2 tane C atomu bağlı ise; o alkol ikincil veya sekonder (2o) alkol olarak sınıflandırılır.
- Alkol molekülünde, -OH grubunun bağlı olduğu C atomuna 3 tane C atomu bağlı ise; o alkol üçüncül veya tersiyer (3o) alkol olarak sınıflandırılır.
Öğretici Örnek:
Aşağıda; birincil-ikincil-üçüncül alkollere örnekler verilmiştir:

Bu bir reklamdır:
Alkollerin Fiziksel ve Kimyasal Özellikleri
- Alkoller, sahip oldukları -OH grubundan dolayı polar bileşiklerdir ve hidrojen bağı kurma yetenekleri vardır.
- Özellikle karbon sayısı az olan alkoller suda çok iyi çözünür ve sulu çözeltilerinde hidrojen bağları kurulur.
- Alkollerdeki -OH sayısı arttıkça kaynama noktası ve sudaki çözünürlük artar.
Metanol (CH3OH)
- Alkollerin en basit üyesi metanoldür.
- Metanol, önceki yıllarda odunun kuru olarak (havasız ortamda, yüksek sıcaklıklarda) damıtılmasıyla elde edilirdi. Bu nedenle metanol, “odun alkolü” olarak da bilinir.
- Günümüzde metanol, yüksek sıcaklık ve basınçta karbonmonoksitin (CO), hidrojen gazı (H2(g)) ile tepkimesinden elde edilir.

- Metanol, oldukça zehirli bir maddedir. Az miktarda metanolün yutulması körlüğe, fazla miktarda yutulması (yaklaşık 30 mL) ölüme yol açmaktadır.
- Metanol zehirlenmesi, buharının uzun süre solunması ya da cildin uzun süre metanole maruz kalması ile de mümkündür.
- Metanolü, koku ve görünüm açısından çok benzediği etanolden ayırt etmek çok zordur.
Etanol (C2H5OH)
- Etanol; şeker kamışı ve mısır gibi bazı bitkilerden elde edilen şekerlerin fermantasyonu sonucu oluşur.
- Fermantasyon, suyla şekerlerin karışımına maya ilave edilerek yapılır.
- Mayanın içerdiği enzimler, basit şekeri (glikoz, C6H12O6 ) etanol ve karbondioksite dönüştürür.

- Canlıların temas ettikleri yüzeylerde bulunan ve insanlarda hastalık yapma özelliğine sahip mikroorganizmaların yok edilmesinde dezenfektan olarak etanol kullanılır. Bu işleme dezenfeksiyon denir.
- Ayrıca canlı dokulardaki zararlı mikroorganizmaların yok edilmesinde de etanol antiseptik madde (mikroorganizmaları yok edici) olarak kullanılmaktadır.
- Saf etanol, endüstriyel kullanım açısından önemli bir kimyasal maddedir. Endüstriyel amaçlı kullanılacak etanol; etenin, asidik ortamda su ile katılma tepkimesinden elde edilir:
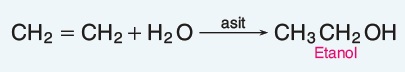
- Etanol, alkil halojenürlerin sulu sodyum hidroksit çözeltisiyle ısıtılması sonucunda meydana gelen yer değiştirme tepkimesiyle de elde edilebilir:
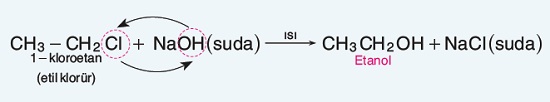
- Etanolün günümüzde en önemli kullanım alanlarından biri de yakıt olarak kullanımıdır.
- Yakıt olarak kullanılan etanol, biyolojik kaynaklardan (mısır, buğday, şeker kamışı gibi) mayalanma yoluyla üretildiği için biyoetanol olarak adlandırılır.
- Etanol, hafif roketli yarış uçaklarında roket yakıtı olarak da kullanılmaktadır.
- Etanol, polar yapıda olduğundan (Hidroksil, hidrofil özelliktedir.), suda çözünebilen önemli bir organik çözücüdür. Bu nedenle çeşitli ilaçlarda, tentürdiyot, boya, esans, parfüm ve birçok kozmetik ürününde çözücü olarak kullanılır.
- 140 °C sıcaklıkta ve asidik ortamda, etanol moleküllerinin tepkimesiyle dietil eter (etoksi etan) elde edilir. Bu tepkime kondenzasyon tepkimesine bir örnektir:

- Etanolün, karboksilik asitlerle tepkimesiyle esterler elde edilir (esterleşme tepkimesi). Örneğin asetik asit ile etanolün tepkimesinden etil asetat elde edilir. Tepkimede açığa çıkan suyun ortamdan uzaklaştırılması tepkimeyi hızlandırır:
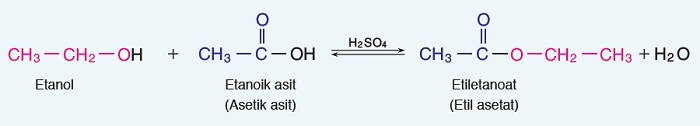
Bu bir reklamdır:
Eterler

- R1 – O – R2 şeklinde gösterilen bileşiklere eter denir. R1 ve R2; aynı veya farklı alkil grupları olabilir.
- Eterlerin genel formülü CnH2n+2O şeklindedir.
- R – O grubuna alkoksi grubu da denir. Eterler, bir alkoksi grubuna bir alkil grubunun bağlanması ile oluşur:
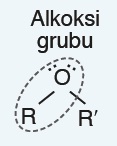
- Su molekülünün, bir hidrojeni alkil grubu (R-) ile yer değiştirirse, alkol bileşiği oluşur; su molekülünün her iki hidrojeni de alkil grupları ile yer değiştirirse eter bileşiği oluşur:
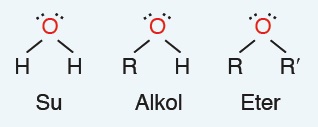
Eterlerin Adlandırılması
- IUPAC adlandırılması, karbon sayısı fazla alkil grubuna bir alkoksi grubu bağlanmış gibi düşünülür.
- Oksijene bağlı daha uzun alkil grubundaki karbon atomlarına, oksijenin olduğu taraftan itibaren numara verilir.
- Daha uzun olan alkil grubu alkan gibi okunur; kısa alkil grubu, alkoksi (metoksi, etoksi…) olarak isimlendirilir.
- Halkalı yapıdaki eterler adlandırılırken, sikloalkanın bir karbon atomunun yerine oksijen geldiği düşünülür ve “oksa” ön eki ile okunur.
- Yaygın adlandırılmada da ise oksijen atomuna bağlı grupların isimleri, alfabetik sıraya göre söylenir ve sonuna “eter” sözcüğü eklenir.
Öğretici Örnek:
Aşağıda verilen eter bileşiklerinin IUPAC ve yaygın isimlerine dikkat edelim:

Bu bir reklamdır:
Öğretici Örnek:
Eterlerin formülü genelde doğrusal yazılır:

Bu bir reklamdır:
Öğretici Örnek:
Kısa ve uzun alkil grubuna dikkat:
Bu bir reklamdır:
Öğretici Örnek:
Alkil grubu ve aril grubu (fenil) de eter oluşturabilir:
Bu bir reklamdır:
Öğretici Örnek:
Alkoksi grubu dal olarak da okunabilir:
Bu bir reklamdır:
Öğretici Örnek:
Uzun olan alkil/aril grubu numaralandırılır:
Bu bir reklamdır:
Simetrik ve Asimetrik Eterler
- R1 ve R2 aynı ise bu etere basit (simetrik) eter denir, R1 ve R2 farklı ise karışık (asimetrik) eter denir.
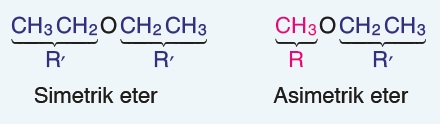
Eterlerin Özellikleri
- Karbon sayıları aynı olan mono alkoller ile eterler izomerlerdir. Bu şekildeki alkol ve eterlere fonksiyonel grup izomerleri denir.
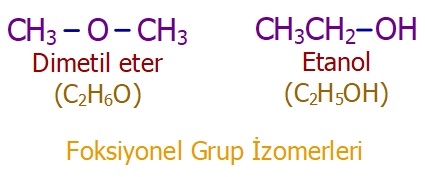
- Eterler; hidrojen bağları kuramaz. Bu yüzden, aynı karbon sayısındaki alkollere göre kaynama noktaları ve sudaki çözünürlükleri daha düşüktür
- Eterler; polar moleküllerdir, karbon sayısı azaldıkça sudaki çözünürlükleri artar.
- Eterler çok reaktif olmadığı için yağlar, mumlar, plastikler ve vernikler gibi organik maddeler için iyi çözücüdür. Dietil eter, çözücü olarak en yaygın kullanılan eterdir.
- Dietil eter; anestezik (bayıltıcı) bir maddedir. Solunum yollarını tahriş eder ve mide bulantısı yapar.
- Eterler çok kararlı bileşiklerdir. Bu yüzden kimyasal tepkimelere girme istekleri azdır.
- Simetrik eterler, alkollerin asidik ortamda ısıtılması ile elde edilir:

- Asimetrik eterler, alkolatların NaOH ile tepkimesinden elde edilir. Bu tepkimeye Williamson Sentezi denir.

Karbonil Bileşikleri (Aldehit ve Ketonlar)
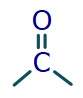
- Karbonil bileşiklerin fonksiyonel grubu, yukarı gördüğünüz karbonil grubudur.
- Karbonil grubunda, bir karbon atomu, bir oksijen atomu ile iki kovalent bağ yapmıştır.
- Fonksiyonel grubu karbonil grubu olan bileşikler; aldehit ve ketonlardır.
- Aldehitlerde, karbonil grubuna en az bir tane H atomu da bağlıdır.
- Ketonlarda, karbonil gurubuna alkil grupları bağlanmıştır.

- Aldehit ve ketonlar, birçok canlı sistemde bulunan, genellikle kendilerine özgü kokuları olan bileşiklerdir.
- Gülün, bademin, tarçının, vanilyanın, limonun, bergamotun, nanenin, portakal çiçeğinin, yasemin çiçeğinin… kendilerine özgü kokuları, içerdikleri aldehit ve ketonlardan kaynaklanmaktadır.
Bu bir reklamdır:
Aldehitlerin Adlandırılması
- Aldehitlerin IUPAC adlandırılmasında, karbonil grubunu içeren en uzun karbon zinciri, ana zincir olarak seçilir ve karbonile en küçük numara gelecek şekilde numaralandırılır.
- Bağlı grupların yerleri ve sayıları belirtilir.
- Ana zincire karşılık gelen alkanın sonuna “-al” son eki getirilir (Aril grubu varsa adlandırma aril grubuna göre yapılır.).
- Aldehitlerin yaygın kullanılan adları da vardır. Bu adlarında, özel adının sonuna -aldehit son eki getirilir.
Aşağıda verilen aldehitlerin IUPAC ve yaygın adlarını inceleyiniz.

Aldehitlerin Fiziksel ve Kimyasal Özellikleri
- Ketonların genel formülü CnH2nO‘dur.
- Aldehitler, karbonil grubunun oksijeninden dolayı polar yapılı bileşiklerdir. Fakat; hidrojen bağı kuramazlar.
- Hidrojen bağı kuramadıkları için, aynı karbon sayısındaki alkol ve karboksilli asitlerden daha düşük kaynama noktasına sahiptirler.
- Sudaki çözünürlükleri karbon sayısı azaldıkça artar.
- Aldehitler kolaylıkla yükseltgenerek organik asitlere (karboksilli asitlere) dönüşürler.
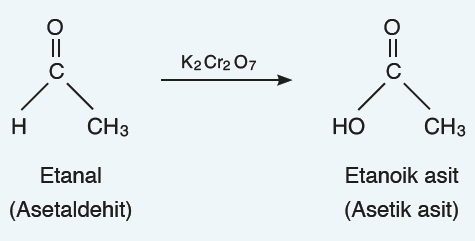
- Fehling ayıracı, bazik ortamda bakır(II) iyonları içeren bir çözeltidir. Aldehitler, fehling çözeltisi ile karboksilik aside yükseltgenirken bakır(II) iyonları bakır(I)’e indirgenir ve kırmızı renkli bakır(I) oksit çökeleği oluşur.

- Tollens ayıracı, amonyaklı gümüş nitrat çözeltisidir. Tollens ayıracı ile tepkimeye giren aldehit, karboksilik aside yükseltgenirken gümüş iyonları metalik gümüşe indirgenir. Bu tepkimenin gerçekleştiği cam kabın iç yüzeyi metalik gümüş ile kaplanır. Cam kaba dıştan bakıldığında ayna gibi görünür. Buna gümüş aynası adı verilir.

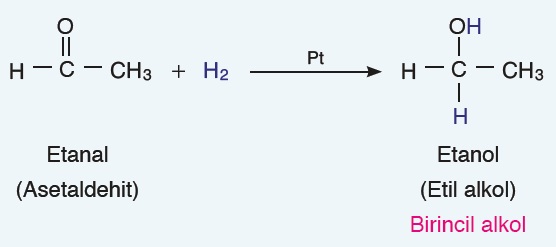
- Aldehit ve ketonların indirgenmesinde hidrojen kaynağı olarak LiAlH4 ve NaBH4 kullanılır. Aldehitler uygun katalizörler ve indirgen maddelerle birincil alkollere indirgenir.
Aşağıdaki örnekte etanal, birincil alkol olan etanole indirgenmiştir:
Ketonların Adlandırılması
- Ketonların IUPAC adlandırılmasında, karbonil grubunun yer aldığı en uzun karbon zincirindeki karbon sayısına karşılık gelen alkanın sonuna “–on” son eki getirilir.
- Karbonil grubuna en küçük sayı gelecek şekilde karbon atomları numaralandırıldığında karbonil grubundaki karbon atomunun numarası belirtilir.
- Ketonların yaygın adlandırılmasında, karbonil grubuna bağlı gruplar alfabetik sıraya göre söylenir.
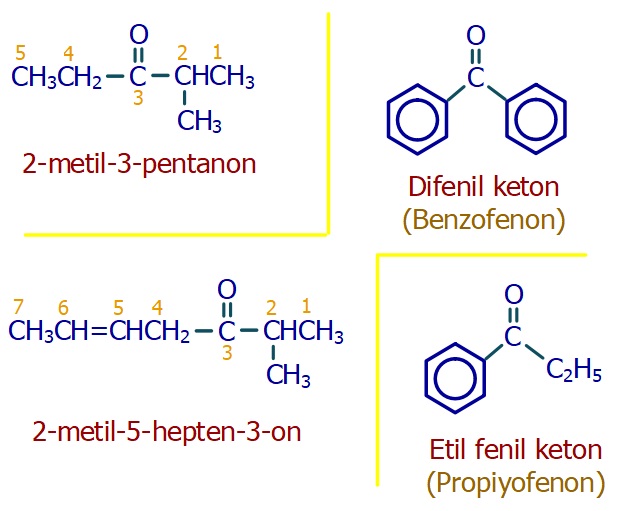
Aşağıda bazı ketonlar ve adları verilmiştir:

Birden fazla karbonil grubu içeren ketonlar şöyle adlandırılır:

Aşağıda, farklı özellikleri olan ketonlar ve isimleri verilmiştir:
Bu bir reklamdır:
Ketonların Fiziksel ve Kimyasal Özellikleri
- Ketonların genel formülü CnH2nO‘dur.
- Aldehitlerin en küçük üyesi tek karbonlu iken (metanal), ketonların en küçük üyesi 3 karbonludur (aseton).
- Karbonil grubuna aynı alkil grupları bağlanınca basit (simetrik) keton, farklı alkil grupları bağlanınca karışık (asimetrik) keton oluşur.
- Ketonlar, karbonil gurubundaki oksijen atomundan dolayı polar yapılı bileşiklerdir.
- Karbon sayısı azaldıkça sudaki çözünürlükleri artar.
- Hidrojen bağı kuramazlar. Bu yüzden karbon sayıları eşit olan alkol ve karboksilli asitlerden daha düşük kaynama noktaları vardır.
- Ketonlar, yükseltgenme tepkimesi vermezler.
- Ketonların indirgenmesinden ikincil alkoller elde edilir:
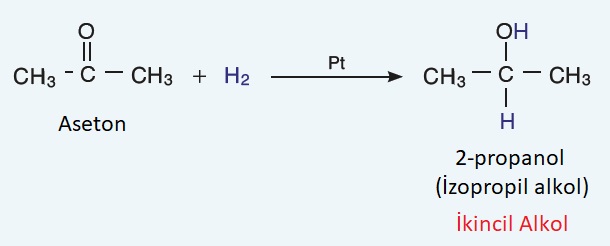
- Karbon sayıları eşit bir aldehit ile bir keton molekülü, birbirinin fonksiyonel grup izomeridir.

Bu bir reklamdır:
Karboksilli Asitler

- Karboksilik asitler, karboksil grubu (–COOH) içeren bileşiklerdir. Genel formülleri RCOOH şeklindedir.
- R grubu, hidrojen atomu olabilir.
- Karboksilik asitlerin fonksiyonel grubu, karboksil grubudur.
- Karboksilli asitlerin genel formülü CnH2nO2‘dir.
- Polikarboksilik asitlerde iki karboksil grubu içerenler dikarboksilik asit, üç karboksil içerenler trikarboksilik asit olarak adlandırılır.
Bu bir reklamdır:
Karboksilli Asitlerin Adlandırılması
- Karboksilik asitlerin IUPAC adlandırılmasında, karboksil grubunun yer aldığı en uzun karbon zincirindeki karbon sayısına karşılık gelen alkanın sonuna “-oik asit” son eki getirilir.
- Numaralandırma işlemine, karboksil grubuna bağlı olan karbon atomuna 1 numara vererek başlanır.
- Başka bağlı gruplar varsa bunların yerleri ve sayıları belirtilerek adlandırma yapılır.
- IUPAC adlarının yanı sıra çok bilinen karboksilik asitlerin yaygın adları da kullanılmaktadır.
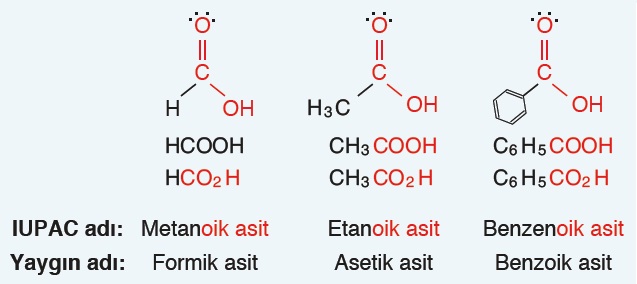
- Yaygın adlandırma için formik asit, asetik asit ve benzoik asit, karboksilik asitler örnek verilebilir.
Öğretici Örnek:
Aşağıda tek karbonlu, iki karbonlu ve aromatik bir karboksilli asit örneği verilmiştir:
Bu bir reklamdır:
Öğretici Örnek:
Dallı bir karboksilli asit örneği:

Bu bir reklamdır:
Öğretici Örnek:
4 ve 5 karbonlu asitler:

Bu bir reklamdır:
Öğretici Örnek:
Fenil grubu dal olarak okunuyor:
Bu bir reklamdır:
Öğretici Örnek:
Aromatik bir asit:
Mono ve Poli Karboksilik Asitler
- Yapısında bir tane karboksil grubu bulunan karboksilik asitler monokarboksilik asitler, birden fazla karboksil grubu bulunanlar polikarboksilik asitler olarak sınıflandırılır.
Öğretici Örnek:
Aşağıda, polikarboksilik asitlere örnekler verilmiştir:

Bu bir reklamdır:
Hidroksiasitler
- Yapısında -OH grubu bulanan karboksilli asitlere hidroksiasitler denir.
- Karboksil grubunun bağlı olduğu karbon atomuna α (alfa), onun yanındakine β (beta), onun yanındakine γ (gama)… karbonu denir.
- Özel adlandırmada numara yerine; α (alfa), β (beta), γ (gama) harfleri kullanılabilir:

Bu bir reklamdır:
Amino Asitler

- Yapısında amino grubu bulanan karboksilli asitlere amino asitler denir.
- Amino grubu bazik özellik gösterir. Bu yüzden amino asitler; hem asidik hem de bazik özellik gösteren bileşiklerdir.
Öğretici Örnek:
Aşağıda, amino asitlere örnekler verilmiştir:

Bu bir reklamdır:
Karboksilli Asitlerin Fiziksel ve Kimyasal Özellikleri
- Karboksil gurubu polar bir gruptur. Bu yüzden karboksilli asitler suda çözünürler.
- Karboksil grubu, Hidrojen bağı (H-bağı) kurma yeteneği olan bir gruptur.
- İki karboksilli asit molekülü arasında iki tane H-bağı kurulur.

- H-bağı kurabildikleri için, H-bağı kuramayan eşit sayıda karbonu olan bileşiklerden daha yüksek kaynama noktasına sahiptirler.
- Karboksil sayısı arttıkça, kaynama noktası artar, sudaki çözünürlük azalır.
- Karboksilli asitler zayıf asitlerdir. Zayıf asitlerin bütün özelliklerini gösterirler.
- Karbon sayısı arttıkça, karboksilli asidin asitlik kuvveti artar.
- Karboksilli asitlerde, alfa karbonuna bağlı yüksek elektronegatif ametalin sayısı arttıkça asitlik kuvveti artar.
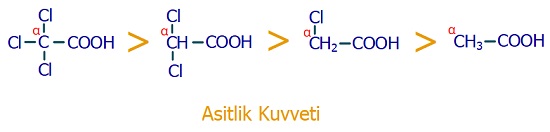
- Karboksilli asitler, diğer asitler gibi aktif metallerle tepkimeye girerler. Sonuçta tuz ve H2 gazı oluşur.
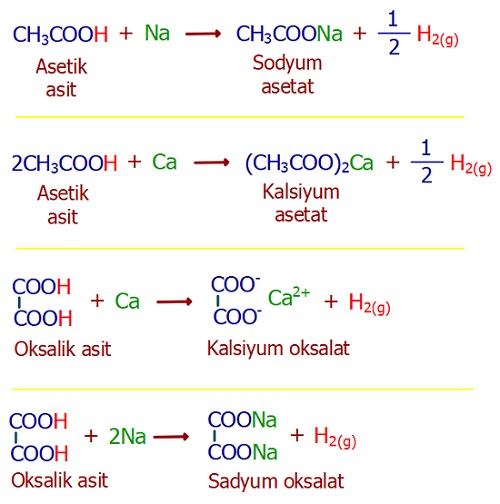
- Karboksilli asitler bir kademe indirgendiğinde aldehitler, iki kademe indirgendiğinde primer alkoller oluşur.

- Bazı karboksilli asitlerin yaygın isimleri şöyledir:

- Karboksilli asitler yükseltgenmezler.
- Formik asit; hem karboksilli asit hem de aldehit özelliği taşır:

- Formik asit:
- Karıncalarda ve ısırgan otunda bulunur.
- Karınca asidi olarak bilinir.
- Kauçuk üretiminde, gıda ve ilaç sanayiinde yaygın olarak kullanılır.
- Asetik asit:
- Sirke asidi olarak bilinir.
- Yaklaşık %5’lik sulu çözeltisi sirke olarak kullanılır.
- Oksalik asit domates ve ıspanakta, bütirik asit tereyağında, propiyonik asit sütte, tartarik asit üzümde, malik asit elmada, sitrik asit limonda bulunur.
- Tartarik asit, malik asit ve sitrik asit meyve asitleri olarak bilinir.
- Sodyum benzoat:
- Benzoik asitin tuzudur.
- Gıda katkı maddesi olarak kullanılır.
- Zararlı mikroorganizmaları öldürür ve bozunmayı engeller.
- Şampuan, tıraş köpüğü ve parfümde kullanılır.
- Folik asit:
- B grubu vitaminlerindendir (B9).
- Folik asitçe zengin bazı besin maddeleri asit, ıspanak gibi yeşil yapraklı sebzelerde bol miktarda bulunur.
- Ayrıca alabalık, böbrek, fıstık, brokoli, lahana, portakal ve tam tahıllılar folik asitçe zengindir.
- DNA sentezinde gerekli olduğu için folik asit, hücre bölünmesinde önemli rol oynar.
- Folik asit eksikliğinde hücreler yeterli şekilde bölünemezler.
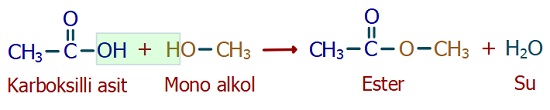
- Karboksilli asitlerin monoalkoller ile tepkimesinden esterler oluşur. Bu tepkime, bir tür kondenzasyon tepkimesidir:
- İki tane monokarboksilli asit molekülünden bir tane su molekülü çekilirse, bir asit anhidrit molekülü oluşur:

Bu bir reklamdır:
Yağ Asitleri
- Canlı organizmalar açısından önemli bir role sahip yağ asitleri de karboksilik asitlere örnektir.
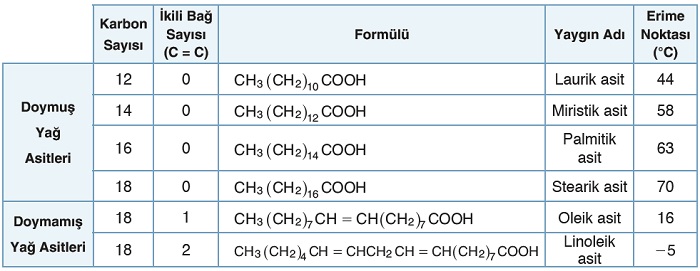
- Yağ asitleri uzun karbon zinciri içeren karboksilik asitlerdir.
- Bunlar doymuş ve doymamış yağ asitleri olmak üzere ikiye ayrılır.
- Yağ asitlerinde karbon zincirindeki karbon atomları arasında ikili bağ (C = C) varsa bu tür yağ asitleri doymamış yağ asitleri olarak sınıflandırılır.
- Karbon atomları arasında sadece tekli bağ (C– C) bulunduran (ikili bağ bulundurmayan) yağ asitleri de doymuş yağ asitleri olarak adlandırılır.
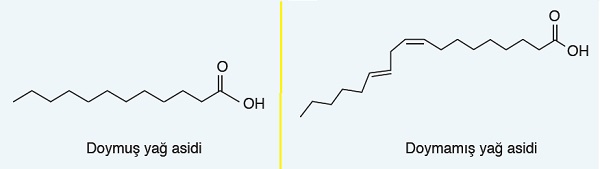
- Doymuş yağ asitlerinin erime noktaları, doymamış yağ asitlerinden daha yüksektir. Çünkü; doymuş yağ asitlerinde van der Waals kuvvetleri daha etkindir.
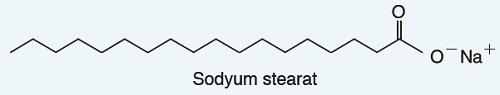
- Sabun, bir yağ asidi tuzudur. Katı sabunun adı sodyum stearattır.
Bu bir reklamdır:
Esterler

- R1CO2R2 ya da R1COOR2 genel formülündeki bileşiklerdir.
- Esterlerde fonksiyonel grup, –CO2 ya da –COO grubudur.

- Esterlerin genel formülü CnH2nO2‘dir.
Esterlerin Adlandırılması
- Esterlerin IUPAC adlandırılmasında:
- fonksiyonel grubun oksijen atomuna bağlı olan alkilin adı belirtilir
- “-COO” grubunun yer aldığı en uzun karbon zincirindeki karbon sayısına karşılık gelen alkanın sonuna -oat son eki getirilir.
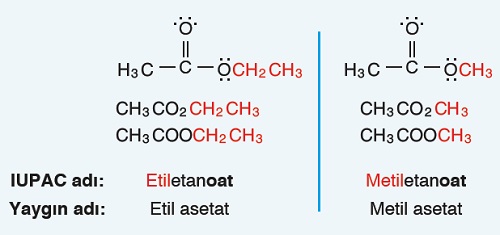
- Yaygın adlandırma için etil asetat ve metil asetat örnek verilebilir.
Öğretici Örnek:
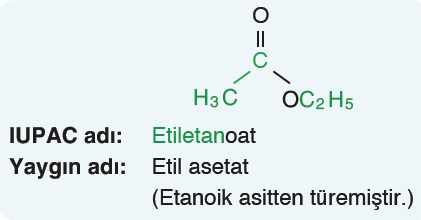
Aşağıdaki örnekleri inceleyiniz.
Bu bir reklamdır:
- Esterler birçok meyvenin güzel kokmasını sağlayan bileşiklerdir. Örneğin muzun kendine has güzel kokusu izopentil asetat, portakalın güzel kokusu ise n -oktil asetat moleküllerinden kaynaklanmaktadır.
Aşağıda, muzun yapısındaki izopentil asetat ile portakalın yapısıdaki n-oktil asetat bileşikleri verilmiştir:

Esterlerin Fiziksel ve Kimyasal Özellikleri
- Karboksilik asit molekülü ile bir alkol molekülü tepkimeye girdiğinde ester elde edilir. Bu tepkimede ester molekülü ile birlikte su molekülü de oluşur. Bu tür tepkimeler esterleşme tepkimeleri olarak bilinir.
- Esterleşme tepkimeleri H2SO4 ya da HCl katalizörlüğünde gerçekleşir.
Aşağıdaki esterleşme tepkimesinde metil etanoat esteri oluşmaktadır:

- Esterler, katı ve sıvı yağların yapısında da doğal olarak bulunur. Yağlar, yağ asitlerinin gliserin molekülü ile esterleşme tepkimesi sonucunda elde edilir.
- Hayvansal yağ olan tristearin, gliserin ve stearik asidin esterleşme tepkimesi sonucunda oluşan bir esterdir.

- Esterler; lanolin, bal mumu ve balsam gibi doğal maddelerin yapısında da bulunmaktadır.

- Lanolin, yünlü hayvanların iklim ve çevre koşullarından korunmak için yağ bezelerinden salgıladıkları mumsu özellikte bir maddedir.
- Özellikle koyun yününden üretilen lanolin;
- kozmetik sektöründe kişisel bakım ürünlerinde kullanılmaktadır. (cilt bakım ürünleri, dudak kremi, yüz kremi gibi).
- Ayrıca yağlayıcı madde, pas önleyici madde ve ayakkabı cilası gibi bazı ticari ürünlerde lanolin kullanılmaktadır.
- Bal mumu, arıların peteklerini yapmak için salgıladıkları yumuşak, sarı renkte ve mumsu bir maddedir.

bal mumunun bileşenlerinden biridir.
b. Bal mumu, mum yapımında da kullanılmaktadır.
- Bal mumu;
- Sadece doğal olarak arılar tarafından üretilen bir madde değildir.
- Sanayide de yapay olarak üretilebilmektedir. Kolay şekil alması nedeniyle kalıp çıkarmada, mum ve heykel yapımında kullanılır.
- Gıda sektöründe bazı gıdaların bozulmasını engellemek ve bu gıdaları nemden korumak için bal mumu kullanılır.
- Bal mumu gıda katkı maddesi olarak da bazı gıda ürünlerinde kullanılmaktadır (gıda kodu, E901).
- Balsam;
- Ester, karboksilik asit ve alkol bileşiklerini içeren bir tür reçinedir. Bazı bitkilerden elde edilen balsam, vücut için gerekli yağları çözmede kullanılır.
- Ayrıca kozmetik sektöründe ve sakız üretiminde de balsam kullanılmaktadır.
- Esterler güzel kokulu ve tatlı maddeler olmalarından dolayı, yapay tatlandırıcılarda ve parfüm üretiminde kullanılır.
- Esterler; boya, vernik ve bazı plastik maddeleri çözmeye de yarar.
- Örneğin etil asetat, boya ve yapıştırıcı maddelere çözücü ve seyreltici etki yapar.
- Şekerlemelerde ve parfümlerde kullanılan etil asetat, tırnak boyasının temizlenmesinde kullanılan asetonun içine de karıştırılır.
Bu bir reklamdır:
Aminler

- Aminler, amonyağın (NH3) organik türevi olarak ifade edilebilir (alkol ve eterlerin suyun organik türevleri olduğu gibi).
- Aminlerin genel formülleri R – NH2‘dir. Bir alkil grubuna (–R), bir amino grubu (-NH2) bağlanması ile aminler elde edilir.
- Amino grubunda azot atomundaki hidrojen atomları yerine alkil grupları da bağlanabilir.
- Aminlerde fonksiyonel grup, ortaklanmamış elektron çifti içeren azot atomudur.

Bu bir reklamdır:
Aminlerin Adlandırılması
- IUPAC adlandırması, bir alkil grubuna, bir amino grubu bağlanmış gibi düşünülür ve alkanlar üzerinden adlandırma yapılır.
- Azot atomuna birden fazla alkil bağlı ise karbon sayısı fazla olan alkile karşılık gelen alkana göre adlandırma yapılır. Diğer alkil grupları, azot atomuna bağlı olduğu için başına “N–” ön eki getirilerek alfabetik sıraya göre söylenir.
- Aminlerin yaygın adlandırılmasında ise azot atomuna bağlı organik gruplar alfabetik sıraya göre söylenir (Aralarında boşluk bırakmadan yazılır.).
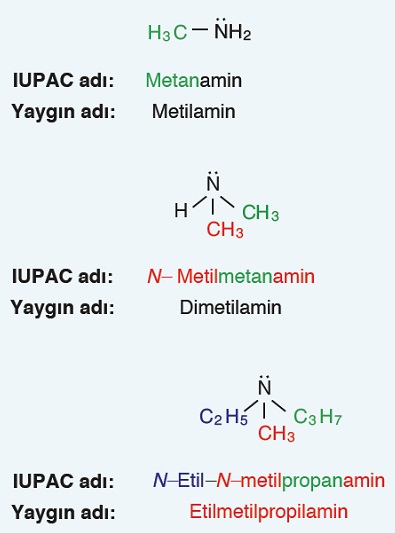
Öğretici Örnek:
Bunun için aşağıdaki örnekleri inceleyiniz.
Bu bir reklamdır: