Kimyasal Tepkimelerde Denge → 2. Bölüm
İçindekiler
DERS
AYT Kimya
Kimya 11
KONU
ÜNİTE VI
KİMYASAL TEPKİMELERDE DENGE
II. Bölüm
2. Bölüm: Dengeyi Etkileyen Faktörler (Le Chatelier Prensibi)
Dersin Özellikleri:
- Seviye: Hiç Bilmeyenler İçin
- Gerekli Bilgiler:
- Kimyasal Denge
- Öğretmen:
- Muzaffer KAYA
Anlatılacak Başlıklar*:
- Le Chatelier Prensibi Nedir?
- Dengeye Etki Eden Faktörler
- Derişimin Dengeye Etkisi
- Sıcaklığın Dengeye Etkisi
- Basın/Hacim Değişiminin Dengeye Etkisi
- Katalizörün Dengeye Etkisi
* Konu anlatımı, örneklerle zenginleştirilmiştir.
Le Chatelier Prensibi Nedir?
- Le Chatelier Prensibine göre; dengedeki (uykudaki) bir tepkime için:
- Dışarıdan bir etkide bulunulduğunda, denge buna bir tepki verir.
- Dengeye etki etmek için şunlar yapılabilir:
- Derişim Değişimi
- Sıcaklık Değişimi
- Basınç Değişimi
- Tepkime, yapılan etkiye zıt yönde olacak şekilde şu tepkilerden birini verir:
- Dengenin sağa (ürünlere) kayması
- Dengenin sola (girenlere) kayması
Mesela:
N2O4(g) + ısı ⇌ 2NO2(g)
- Tepkimesi sabit hacimli kapta ve dengede iken:
- Etki: Kaba N2O4 eklersek (derişimi artarsa),
- Tepki: Denge ürünlere (sağa) kayar.
- Etki: Kaba NO2 eklersek (derişimi artarsa),
- Tepki: Denge girenlere (sola) kayar.
- Etki: Kaptan N2O4 gazı çekersek (derişimi azalırsa),
- Tepki: Denge denge girenlere (sola) kayar.
- Etki: Kabı ısıtırsak (sıcaklık artarsa),
- Tepki: Denge ürünlere (sağa) kayar.
- Etki: Kaba N2O4 eklersek (derişimi artarsa),
Dengeye Etki Eden Faktörler
1. Derişimin Dengeye Etkisi
- Dengedeki bir tepkimede:
- Derişimi artan madde dengeyi karşı tarafa iter.
N2O4(g) ⇌ 2NO2(g)
- Bu tepkime sabit V ve T’de ve dengede iken, kaba N2O4 eklenirse, derişim-zaman grafiği şöyle olur:
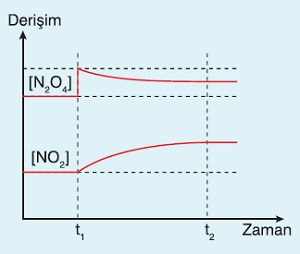
Örnek:
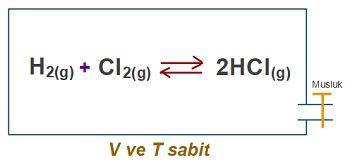
Şekildeki tepkime dengede iken kaba bir miktar Cl2 gazı ekleniyor.
Buna göre, ikince denge kurulana kadar tepkimedeki maddelerin derişimleri nasıl değişir?
Dengeye Etki Eden Faktörler
2. Sıcaklığın Dengeye Etkisi
- Sıcaklık, denge sabitini değiştirebilen tek faktördür.
- Dengedeki bir tepkimede, sıcaklık değişimi ile tepkime:
- Ürünlere kayarsa:
- Denge sabiti (Kc) büyür.
- Girenlere kayarsa:
- Denge sabiti (Kc) küçülür.
- Ürünlere kayarsa:
- Sıcaklık artarsa ileri ve geri tepkimeler:
- hızlanır.
- hız sabitleri artar.
- Sıcaklık düşerse bunların tam tersi gerçekleşir.
Mesela:
N2O4(g) + ısı ⇌ 2NO2(g)
- Endotermik tepkime dengede iken:
- Kaba ısı verilirse, denge ürünlere kayar.
- Kap soğutulursa, denge girenlere kayar.
2NO2(g) ⇌ N2O4(g) + ısı
- Ekzotermik tepkime dengede iken:
- Kaba ısı verilirse, denge girenlere kayar.
- Kap soğutulursa, denge ürünlere kayar.
Dengeye Etki Eden Faktörler
2. Sıcaklığın Dengeye Etkisi
N2O4(g) + ısı ⇌ 2NO2(g)
- Tepkimesine ısı verirsek, ürünlere kayar ve derişim zaman grafiği şöyle çizilir:

Örnek:
CH4(g) + O2(g) ⇌ CO2(g) + 2H2O(g) ΔH = -436 kj/mol
Yukarıdaki tepkime, kapalı ve sabit hacimli bir kapta dengede iken, tepkime kabı bir miktar ısıtılıyor ve daha yüksek bir sıcaklıkta tekrar denge kurması sağlanıyor.
Buna göre, aşağıdaki yargılardan hangisi yanlıştır?
A) Denge girenlere (sola) kayar.
B) Denge sabiti büyür.
C) Kaptaki O2(g)derişimi artar.
D) Kaptaki CO2(g) derişimi düşer.
E) CH4(g) derişimi azalan H2O(g) derişiminin yarısı kadar artar.
Dengeye Etki Eden Faktörler
3. Basınç/Hacim Değişiminin Dengeye Ektisi
- Gazlı tepkimelerin dengesinde hacimle oynanırsa basınç da değişir.
- Dengedeki bir tepkimede, tepkime kabının hacmi:
- Düşerse, kabın basıncı artar.
- Denge basıncı azaltmak için gaz sayısının az olduğu tarafa kayar.
- İleri ve geri tepkime hızlanır.
- Artarsa, kabın basıncı düşer.
- Denge basıncı arttırmak için gaz sayısının çok olduğu tarafa kayar.
- İleri ve geri tepkime yavaşlar.
- Düşerse, kabın basıncı artar.
Mesela:
N2O4(g) ⇌ 2NO2(g)

- Yandaki tepkime pistonlu kapta dengede iken, piston aşağıya itilirse:
- Basınç artar.
- Denge basıncı azaltmak ister.
- Bu yüzden gazların az olduğu tarafa yani girenlere kayar.
Dengeye Etki Eden Faktörler
3. Basınç/Hacim Değişiminin Dengeye Ektisi
N2O4(g) ⇌ 2NO2(g)
- Tepkimesi dengede iken kabının hacmi azaltılırsa, bu olayın Derişim-zaman grafiği şöyle olur:

Örnek:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Tepkime, ideal pistonlu bir kapta dengedeyken, sıcaklık değişmeden, piston belli bir miktar aşağı itilerek tekrar sabitleniyor.
Bu olay için hangisi doğru değildir?
A) Tepkime ürünlere kayar.
B) İkinci bir denge kurulur.
C) Kaptaki toplam derişim artar.
D) Kaptaki toplam mol sayısı artar.
E) Kaptaki toplam basınç artar.
Dengeye Etki Eden Faktörler
4. Katalizörün Dengeye Ektisi
- Dengenin daha hızlı kurulmasını sağlar.
- Kc ve Kp sabitlerini değiştirmez.
- İleri ve geri tepkimeyi hızlandırır.
- İleri ve geri tepkimenin hız sabitlerini arttırır.
- Dengedeki bir tepkimeye, etki etmez.
Örnek:

Şekildeki kapta, sabit bir hacim ve sıcaklıkta 1M H2, 4M Cl2 ve 4M HCl dengededir. Tepkime kabından 3M Cl2 gazı çekilip, aynı sıcaklık ve hacimde dengenin tekrar kurulması bekleniyor.
Buna göre, kurulan ikince dengede, HCl gazının derişimi kaç Molar olur?

Kimyasal Tepkimelerde Denge
II. Bölüm
Dengeyi Etkileyen Faktörler (Le Chatelier Prensibi)
Bitti 🙁