Karbon Kimyasına Giriş → 3. Bölüm
İçindekiler
- 3. Bölüm – Doğada Karbon
- Karbon Elementinin Genel Özellikleri
- Karbon Elementinin Genel Özellikleri
- Karbon Elementinin Bağ Yapma Özelliği
- Karbon Elementinin Bağ Yapma Özelliği
- Karbon Elementinin Allotropları
- Karbon Elementinin Allotropları
- Elmas
- Grafit
- Grafen
- Fullerenler (C60)
- Nanotüpler
- Karbon Elementinin Allotropları
DERS
AYT Kimya
Kimya 12
KONU
ÜNİTE II
KARBON KİMYASINA GİRİŞ
III. Bölüm
3. Bölüm – Doğada Karbon
Dersin Özellikleri:
- Seviye: Hiç Bilmeyenler İçin
- Gerekli Bilgiler:
- Karbon Kimyasına Giriş – II. Bölüm
- Öğretmen:
- Muzaffer KAYA
Anlatılacak Başlıklar*:
- Karbon Elementinin Genel Özellikleri
- Karbon Atomunun Bağ Yapma Özelliği
- Karbon Elementinin Allotropları
- Elmas
- Grafit
- Grafen
- Fullerenler (C60)
- Nanotüpler
* Konu anlatımı, örneklerle zenginleştirilmiştir.
Karbon Elementinin Genel Özellikleri
- Karbon (C) elementi:
- Periyodik sistemin 4A grubu (14. grup) 2. periyotunda bulunur.
- Ametaldir.
- Canlılığın temel elementidir.
- Yer yüzünde canlılık, C elementi üzerinden ortaya çıkmış ve devam etmektedir.
- Canlı organizmalardaki bileşikler, organik bileşiklerdir, yani karbon bileşikleridir.
- Vücudumuzda, oksijenden sonra en çok bulunan element karbon elementidir.
- Bağ yapma yeteneği yüksektir.
- Tek başına, diğer bütün elementlerden daha çok sayıda bileşiği vardır.
- Bu yüzden, doğada karbon atomu, farklı şekillerde karşımıza çıkabilmektedir.

Karbon Elementinin Genel Özellikleri
Örnek:
Saynur hanım, karbon elementinin ne kadar özel bir element olduğunu anlatırken aşağıdaki ifadeleri kullanmış fakat bazı hatalar yapmıştır.
I) Karbon elementi yaşamın temel elementidir.
II) Karbon elementi bir 4A grubu ametalidir.
III) Anorganik kimyaya, “karbon kimyası” da denmektedir.
IV) Bütün organik bileşiklerin ortak elementi karbon elementidir.
V) Uzun yıllar, karbon temelli bileşiklerin, suni yollarla üretilemeyeceğine inanılmıştır.
Buna göre, Saynur hanım, karbon elementini tarif ederken hangi hatalı bilgiyi vermiştir?
A) I
B) II
C) III
D) IV
E) V
Karbon Elementinin Bağ Yapma Özelliği
- Karbon bileşiklerinde toplam 4 tane kovalent bağ yapar.
- Bu bağların içinde:
- Tekli kovalent bağlar
- İkili kovalent bağlar
- Üçlü kovalent bağlar olabilir.
- Bu bağların içinde:

Örnek
Bileşik ne olursa olsun, karbon 4 kovalent kurmalıdır.

Karbon Elementinin Bağ Yapma Özelliği
Örnek:
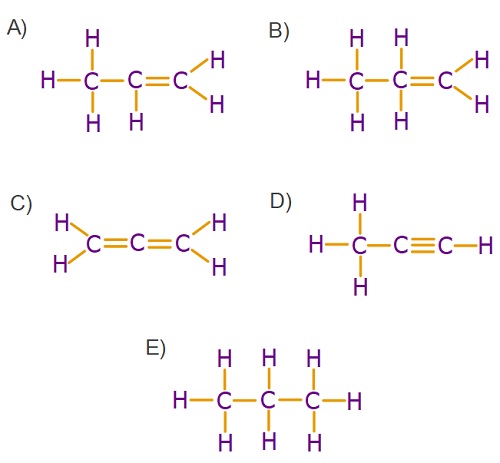
Nagehan, performans ödevi olarak, bazı organik bileşiklerin yapı formüllerini çizmiştir. Öğretmeni, formüllerden birinde hata olduğunu, tabiatta böyle bir molekül olmadığın söylemiştir.
Nagehan’ın ödevinde hazırladığı moleküller aşağıdaki gibi olduğuna göre, hangi molekül hatalı olmuştur?
Karbon Elementinin Allotropları
Allotrop Nedir?
- Aynı atomların farklı şekillerde dizilmesi ile oluşan farklı maddelere allotrop denir.

Allotropların Özellikleri
- Aynı elementtirler.
- Fiziksel özellikleri (renk, koku, tat, EN, KN, özkütle…) farklıdır.
- Bazı kimyasal özellikleri farklıdır.
- Aynı maddeler ile tepkimeye girdiklerinde aynı ürünleri oluştururlar.
- Tepkimelere girme istekleri farklıdır.
Karbonun Allotropları
- Karbon elementinin en bilinen allotropları şunlardır:
- Doğal allotropları:
- Elmas
- Grafit
- Yapay allotropları:
- Grafen
- Fullerenler (C60)
- Nanotüpler
- Doğal allotropları:
Karbon Elementinin Allotropları
Örnek:
Poyraz, bir kır gezisi esnasında dikkatini çeken iki maddeyi yanına almış ve ilk fırsatta, bu maddeleri, analiz için bir laboratuvara göndermiştir. Laboratuvarda yapılan inceleme sonucunda, bu iki maddenin özellikleri için şu bilgiler verilmiştir:
I) Maddelerin fiziksel özellikleri farklıdır.
II) Maddeler aynı atomlardan oluşmaktadır.
III) Maddelerin kristalleri incelendiğinde, farklı geometrik şekillere sahip olduğu görülmüştür.
IV) Maddelerin yanma ürünlerinin aynı olduğu görülmüştür.
Buna göre bu sonuçlardan hangisi ya da hangileri, bu iki maddenin allotrop maddeler olduğunu kesin olarak kanıtlamak için yeterlidir?
A) Yalnız II
B) I ve II
C) II ve III
D) II ve IV
E) I, II ve IV
Elmas
- Saydamdır.
- Elektriği iletmez.
- Isıyı iyi iletir.
- Karbon atomları:
- 4 tane tekli kovalent bağ kurmuştur.
- sp3 hibritleşmesi yapmıştır.
- Düzgün dörtyüzlü şeklinde dizilmiştir.
- Doğal maddeler içinde, en sertidir.
- İyi bir kesici ve aşındırıcıdır.
- 850 oC’de yanar, 3500 oC’de erir.
- Erime noktası grafitten daha yüksektir.
- Her elmasın kristalleri farklıdır.
- Kristal dizilimi birbirinin aynı olan 2 tane elmas yoktur.
- Grafitten, yapay olarak elde edilebilmektedir.


Grafit
- Yağlıdır.
- Siyah-çelik rengi arası renktedir.
- Yumuşaktır.
- Kağıt üzerinde iz bırakır.
- Kurşun kalemlerin ucu, kil karıştırılarak sertleştirilmiş grafittir.
- Elektrik akımın iletir.
- Makine yağlayıcısı olarak kullanılır.
- Sıcaklığa dayanıklıdır.
- Uzay araçlarında ısı kalkanı olarak kullanılır.

- Kağıt destesi gib üst üste dizilmiş tabakalardan oluşur.
- Bu tabakaların her birine grafen denir.
- Grafen tabakalar arasında Van der Waals etkileşimleri etkilidir.

Grafen
- Karbonun yapay bir allotropudur.
- Grafiti oluşturan tabaklardan her biridir.
- Isı ve elektrik iletkenliği üst düzeydedir.
- İki boyutlu ve saydam bir tabakadır, elektronik kağıt olarak da isimlendirilir.
- Çelikten 6 kat daha sert ve hafif, 13 kat daha esnektir.
- Şu ürünlerin üretilebilmesini sağlayacaktır:
- Süper küçük bilgisayar
- Kirlenmeyen kumaş
- Deri altına yerleşebilen tıbbi cihazlar…
- Süperkapasitörler (pil sorununu çözebilir)
- Radyoaktif atıkların daha kolay temizlenmesi
- Daha sağlam ve hafif uçaklar

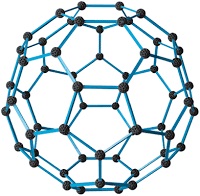
Fullerenler (C60)
- C elementinin yapay bir allotroplarıdır. (Doğal olanlar da keşfedilmiştir.)
- Fulleren adı, Richard Buckminster Fuller (1895-1983)’den almıştır.
- Top, tüp, çubuk ve halka şeklinde olabilirler.
- Asal yapıda maddelerdir, kimyasal etkinlikleri yoktur.
- Karbonlar; beşgen, altıgen veya yedigen şeklinde dizilebilirler.
- Bazı kullanım alanları şunlardır.
- Güneş pilleri
- Hidrojen yakıt depoları
- Kurşun geçirmez yelek yapımı
- Süper iletken
- HIV virüsünün teşhisi
- Kanser tedavisi
Nanotüpler
- Grafen tabakalarının tüp şeklinde yuvarlanması ile elde edilmektedir.
- Esnek ve sağlamdırlar.
- Sumi Lijima keşfetmiştir. (Japon-1991)
- Nano (10-9) teknolojinin gelişmesinde önemlidir.
- Çok düşük sıcaklıklarda bile elektrik akımını ilettirler, “süper iletken“dirler.
- Elmastan daha sert, çelikten daha sağlamdır.
- Bazı kullanım alanları şunlardır:
- Biyosensör yapımı
- Nanoteknoloji
- Dokunmatik ekran
- Taramalı, tünelleme mikroskopları
- Organik güneş pilleri
- Hidrojen pilleri
- Zehirli gaz dedektörü
- Hidrojen depolama
- Çok küçük elektronik cihaz yapımı
- Leke tutmaz kumaş yapımı

Karbon Elementinin Allotropları
Örnek:
Evliya Çelebi, 17. yüzyılda yaşamış ve bir çok ülke gezerek tecrübelerini “Seyahatname” adlı bir kitapta toplamış bir gezgindir.
Buna göre, Evliya Çelebi’nin gezdiği ülkelerde, aşağıdaki maddelerden hangisini hiç bir zaman görmediği söylenebilir?
A) Kömür
B) Elmas
C) Grafit
D) Fullerenler
E) Altın

KARBON KİMYASINA GİRİŞ
III. Bölüm
(Doğada Karbon)
Bitti 🙁