Karbon Kimyasına Giriş → 2. Bölüm
İçindekiler
- 2. Bölüm: Basit Formül ve Molekül Formülü
- Formül Nedir?
- Organik Bileşiklerin Formülleri
- 1. Molekül (Bileşik) Formülü
- 2. Basit (Kaba-Amprik) Formül
- 2. Basit (Kaba-Amprik) Formül
- 3. Açık Formül (Yapı Formülü)
- 4. Yarı Açık Formül
- 5. Çizgi-Bağ (İskelet) Formülü
- 5. Çizgi-Bağ (İskelet) Formülü
- 5. Çizgi-Bağ (İskelet) Formülü
- Kaba Formül Bulma Problemleri
- Kaba Formül Bulma Problemleri
- Kaba Formül Bulma Problemleri
DERS
AYT Kimya
Kimya 12
KONU
ÜNİTE II
KARBON KİMYASINA GİRİŞ
II. Bölüm
2. Bölüm: Basit Formül ve Molekül Formülü
Dersin Özellikleri:
- Seviye: Hiç Bilmeyenler İçin
- Gerekli Bilgiler:
- Kimyasal Hesaplamalar
- Öğretmen:
- Muzaffer KAYA
Anlatılacak Başlıklar*:
- Formül Nedir?
- Organik Bileşiklerin Formülleri
- Molekül Formülü
- Basit Formül ( Kaba veya Ampirik formül de denir.)
- Açık Formül
- Yarı Açık Formül
- Çizgi-Bağ (İskelet) Formülü
- Formül Bulma Problemleri
* Konu anlatımı, örneklerle zenginleştirilmiştir.
Formül Nedir?
Formül Nedir?
- İyonik bileşiklerde:
- Molekülleri yok, kristalleri vardır.
- Formülleri, kristallerinin birim hücresinde bulunan iyonların oranını gösterir.
- Kovalent bileşiklerde:
- Molekülleri vardır.
- Formülleri, bir molekülde bulunan atomları ve sayılarını gösterir.
CH4 Molekülü
- CH4 bileşiği kovalenttir.
- Molekülleri vardır.
- Bir molekülünde:
- 1 C atomu 4 H atomu vardır.

Organik Bileşiklerin Formülleri
- Bir bileşiğin formülünü göstermenin birden fazla yolu vardır. Bunlar:
- Molekül Formülü
- Basit Formül (Kaba veya Ampirik formül)
- Açık Formül
- Yarı Açık Formül
- Çizgi-Bağ (İskelet) Formülü
1. Molekül (Bileşik) Formülü
- Bir tane molekülde, hangi atomların kaçar tane bulunduğu gösteren formüldür.
- Aşağıda bazı bileşiklerin molekül formülleri verilmiştir:
- H2O (Su)
- CH4 (Metan)
- C2H2 (Asetilen)
- C2H6 (Etan)
- C4H10 (Bütan)
- C2H5OH (Etil alkol)
2. Basit (Kaba-Amprik) Formül
- Molekül formüllerinin sadeleştirilmesi ile elde edilir.
- Basit formülün başlıca özellikleri:
- Kaç ile sadeleştiği bilinmiyorsa molekül formülüne ulaşılamaz.
- Bileşikteki oranlar değişmez.
- Farklı bileşiklerin basit formülleri aynı da olabilir.
- Bazı bileşiklerde, molekül formülü ile basit formül aynı olabilir.
Bazı bileşiklerin molekül ve kaba formülleri şöyledir:

2. Basit (Kaba-Amprik) Formül
Örnek
Aşağıdaki bileşiklerden hangisinin molekül formülüyle basit formülü aynı değildir?
A) C5H12
B) CH₃COOH
C) C₂H₅OH
D) C₃H₈
E) C₃H₆O₂
3. Açık Formül (Yapı Formülü)
- Molekül, kovalent bağları ile gösterilir.
- Kovalent bağ; atomların arasına çizilen kısa bir çizgi ile (“―“) gösterilir.
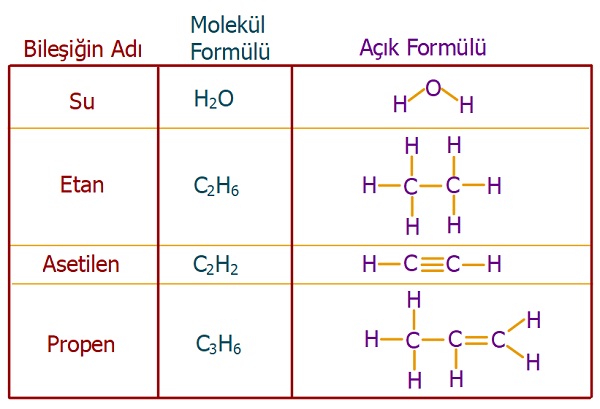
4. Yarı Açık Formül
- Açık formüle benzer fakat:
- H atomunun bağları gösterilmez.
- Bazen C atomlarının da bağları gösterilmeyebilir.
C3H8 (propan) bileşiğinin farklı gösterimleri:
Molekül Formülü
C3H8
Açık Formülü

Yarı Açık Formülü

5. Çizgi-Bağ (İskelet) Formülü
- Genellikle, sadece karbonlar arası kovalent bağlar görünür.
- Yapı formülünden şunlar silinerek elde edilir:
- C atomları
- C atomlarına bağlı H atomları
- C―H bağları
- H’nin bağları
- Geriye kalan bağlar zikzaklı çizilir.
C4H8 (bütan) bileşiğinin farklı gösterimleri:
Molekül Formülü
C4H10
Açık Formülü

Çizgi-Bağ Formülü

5. Çizgi-Bağ (İskelet) Formülü
Örnek
Aşağıda yapı formülü verilen bileşiğin çizgi-bağ formülünü yazınız.

5. Çizgi-Bağ (İskelet) Formülü
- Çizgi-bağ formüllerinde, C ve H dışındaki ametaller görünür.
- C atomu dışındaki atomlara bağlanan H atomları da görünür.
Örnek
Aşağıda yapı formülü verilen bileşiğin çizgi-bağ formülünü yazınız.

Kaba Formül Bulma Problemleri
Kaba formül bulmanın iki yolu vardır. Bu yollar şunlardır:
- Elementlerin miktarları belli ise:
- Bileşikteki her bir elementin teker teker mol sayısı hesaplanır.
- Hesaplanan mol sayıları formülde, elementlerinin altına yazılır.
- Sayılar tam değilse en küçük tam sayılara çevrilir.
Örnek
Sadece karbon ve hidrojenden oluşan bir bileşiğin 3,2 gramında 2,4 gram C elementi tespit edilmiştir.
Buna göre bu bileşiğin kaba formülü nedir? (C: 12 g/mol, H: 1 g/mol)
Kaba Formül Bulma Problemleri
Kaba formül bulmanın ikinci yolu:
- Denkleşmiş kimyasal tepkime denklemi verilir ya da tarif edilir ise:
- Tepkime denklemi yazılır.
- Denkleştirme kurallarına göre bileşiğin formülünü bulunur.
Örnek
X + 3O2 → 2CO2 + 3H2O
Yukarıda verilen tepkimeye göre X bileşiğinin formülü nedir?
Kaba Formül Bulma Problemleri
- Kaba formülü ve mol ağırlığını biliyorsak, molekül formülünü de bulabiliriz.
Örnek
Karbon ve hidrojenden oluşan bir organik bileşik analiz edildiğinde, kütlece %10 hidrojen elementinden oluştuğu anlaşılıyor.
Bu bileşiğin mol ağırlığının 80 olduğu bilindiğine göre, molekül formülü nedir? (C: 12 g/mol, H: 1 g/mol)

Karbon Kimyasına Giriş
II. Bölüm
(Basit Formül ve Molekül Formülü)
Bitti 🙁